题目内容
已知aL硫酸铝溶液中,含有27g A13+,取0.5aL硫酸铝溶液稀释至2aL,则稀释后溶液中SO42ˉ的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度的相关计算
专题:计算题
分析:n(A13+)=
=1mol,原来硫酸铝溶液中c(A13+)=
=
mol/L,溶液稀释前后溶质的物质的量不变,根据n=CV知,溶液体积增大4倍,则溶液物质的量浓度降为原来的
,硫酸铝中铝离子和硫酸根的浓度之比等于其系数之比.
| 27g |
| 27g/mol |
| 1mol |
| aL |
| 1 |
| a |
| 1 |
| 4 |
解答:
解:n(A13+)=
=1mol,原来硫酸铝溶液中c(A13+)=
=
mol/L,溶液稀释前后溶质的物质的量不变,根据n=CV知,溶液体积增大4倍,则溶液物质的量浓度降为原来的
,所以稀释后铝离子浓度为
mol/L,硫酸铝中铝离子和硫酸根的浓度之比等于其系数之比,所以稀释后c(SO42ˉ)=
×3mol/L=
mol/L,故选A.
| 27g |
| 27g/mol |
| 1mol |
| aL |
| 1 |
| a |
| 1 |
| 4 |
| 1 |
| 4a |
| ||
| 2 |
| 3 |
| 8a |
点评:本题考查物质的量浓度计算,明确盐溶液中各微粒浓度与其系数之间的关系式是解本题关键,溶液具有均一性和稳定性,同一溶液浓度与溶液体积无关,为易错点.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
下列反应的离子方程式书写正确的是( )
A、用惰性电极电解MgCl2溶液2Cl-+2H2O
| ||||
| B、向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2HCO3-+2OH-═CO32-+CaCO3↓+2H2O | ||||
| C、次氯酸钙溶液中通入过量的CO2:Ca2++3ClO-+H2O+CO2═CaCO3↓+2HClO | ||||
| D、氢氧化铁溶于碘化氢溶液:Fe(OH)3+3H+═Fe3++3H2O |
下列有关指定装置图的说法中正确的是( )


| A、用图1作为气体发生装置,液体由分液漏斗加入与烧瓶中固体反应,产生的难溶于水的气体用排水法测量气体体积时,排出的水的体积扣除分液漏斗加入的液体体积即为产生气体的体积 |
| B、用图2测量难溶于水的气体体积时,如果气体滞留在烧瓶中,会导致测定的氢气体积偏小 |
| C、用图3可以完成喷泉实验 |
| D、图4可以“随开随用,随关随停”地用于一些气体的制备 |
下列说法中错误的是( )
| A、NaCl溶液焰色反应呈黄色 |
| B、NH3能使湿润的红色石蕊试纸变蓝 |
| C、漂白粉的主要成分是次氯酸钙和氯化钙 |
| D、进行蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
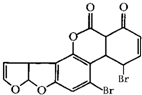 某有机物是一种强致癌物,其结构如图所示.1mol该化合物在一定条件下分别与H2、NaOH溶液反应,最多消耗H2和NaOH的物质的量分别为( )
某有机物是一种强致癌物,其结构如图所示.1mol该化合物在一定条件下分别与H2、NaOH溶液反应,最多消耗H2和NaOH的物质的量分别为( )| A、6mol、4mol |
| B、7mol、4mol |
| C、7mol、5mol |
| D、6mol、5mol |
将下列固体物质溶于水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是( )
①胆矾 ②氯化铝 ③硫酸铝 ④纯碱 ⑤小苏打 ⑥氯化铜.
①胆矾 ②氯化铝 ③硫酸铝 ④纯碱 ⑤小苏打 ⑥氯化铜.
| A、①③④ | B、①②③④ |
| C、全部 | D、③④ |
下列溶液氯离子的物质的量浓度与50mL 2mol?L-1氯化铝溶液中氯离子的物质的量浓度相等的是( )
| A、150 mL 1 mol?L-1氯化钠溶液 |
| B、75 mL 1.5 mol?L-1氯化钙溶液 |
| C、150 mL 3 mol?L-1氯化钾溶液 |
| D、50 mL 3 mol?L-1氯化镁溶液 |

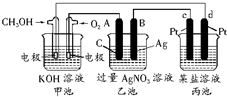 如图所示的装置中,甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.
如图所示的装置中,甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.