题目内容
13.工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3).其工业流程如下: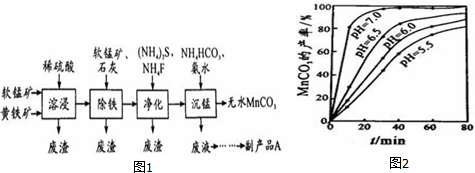
回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有(写一条)搅拌、适当升高温度、研磨矿石、适当提高稀硫酸的浓度等.
(2)除铁工序中,在加入石灰调节溶液的pH前,加入适量的软锰矿,其作用是(用离子方程式表示)MnO2+2Fe2++4H+=2Fe3++Mn2++2H2O.
(3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质.若测得滤液中c(F-)=0.01mol•L-1,滤液中残留的c(Ca2+)=1.46×10-6mol•L-1〔已知:Ksp(CaF2)=1.46×10-10〕.
(4)沉锰工序中,298K、c(Mn2+)为1.05mol•L-1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如图2所示.根据图中信息得出的结论是pH等于7.0时反应速率最快,且MnCO3的产率最高.
(5)从沉锰工序中得到纯净MnCO3的操作依次是过滤、洗涤、干燥.
(6)副产品A的化学式是(NH4)2SO4.
分析 (1)通过搅拌、适当升高温度、研磨矿石、适当增大酸的浓度等,可以提高溶浸工序中原料的浸出率;
(2)主要成分是FeS2的黄铁矿在酸浸过程中产生亚铁离子,因此流程第二步除铁环节的铁应该转化铁离子才能更好除去,所以需要加入氧化剂软锰矿使残余的Fe2+转化为Fe3+;
(3)由于流程第二步加入了石灰引入了Ca2+杂质,因此除去溶液中的Cu2+、Ca2+等杂质可分别使用(NH4)2S和NH4F,生成CuS、CaF沉淀除去,根据已知氟化钙的溶度积和c(F-),可求c(Ca2+);
(4)根据沉锰的图象可知,pH越大得到的MnCO3的产率越高,且需要的时间越短,且在pH=7时,有更好的效果;
(5)从沉锰工序中得到纯净MnCO3,只需将沉淀析出的MnCO3过滤、洗涤、干燥即可得到碳酸锰;
(6)得到的滤液中还有大量的铵根离子和硫酸根离子没有反应,据此判断副产品.
解答 解:(1)提高浸取率的措施可以是搅拌、适当升高温度、研磨矿石、适当增大酸的浓度等,
故答案为:搅拌、适当升高温度、研磨矿石、适当提高稀硫酸的浓度等;
(2)主要成分是FeS2的黄铁矿在酸浸过程中产生亚铁离子,因此流程第二步除铁环节的铁应该转化铁离子才能更好除去,所以需要加入氧化剂软锰矿使残余的Fe2+转化为Fe3+,离子方程式为MnO2+2Fe2++4H+=2Fe3++Mn2++2H2O,再加入石灰调节pH值使Fe3+完全沉淀,
故答案为:MnO2+2Fe2++4H+=2Fe3++Mn2++2H2O;
(3)由于流程第二步加入了石灰引入了Ca2+杂质,因此除去溶液中的Cu2+、Ca2+等杂质可分别使用(NH4)2S和NH4F,生成CuS、CaF沉淀除去,根据已知氟化钙的溶度积和c(F-)可知:c(Ca2+)=$\frac{K{\;}_{sp}(CaF{\;}_{2})}{c{\;}^{2}(F{\;}^{-})}$=$\frac{1.46×10{\;}^{-10}}{0.01{\;}^{2}}$=1.46×10-6mol•L-1,
故答案为:1.46×10-6mol•L-1;
(4)从沉锰的图象可以看出,在已给的几个pH值条件下,pH越大得到的MnCO3的产率越高,且需要的时间越短,且在pH=7时,有更好的效果,因此结论是pH等于7.0时反应速率最快,且MnCO3的产率最高,
故答案为:pH等于7.0时反应速率最快,且MnCO3的产率最高;
(5)从沉锰工序中得到纯净MnCO3,只需将沉淀析出的MnCO3过滤、洗涤、干燥即可,
故答案为:过滤;干燥;
(6)得到的滤液中还有大量的铵根离子和硫酸根离子没有反应,因此可以制的副产品为:(NH4)2SO4,
故答案为:(NH4)2SO4.
点评 本题通过碳酸锰的制备,考查了物质制备实验方案的设计方法,题目难度较大,明确制备流程及相应的反应原理为解答关键,试题涉及的知识点较多、综合性较强,充分考查了学生的分析、理解能力及化学实验能力.

 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案| A. | 可能由pH=2的盐酸与pH=12的氨水等体积混合而成 | |
| B. | 该溶液可能由等物质的量浓度的盐酸和氨水等体积混合而成 | |
| C. | 加入适量氨水,溶液中离子浓度可能为:c (NH4+)>c (Cl-)>c (OH-)>c(H+) | |
| D. | 该溶液中c (NH4+)=c (Cl-)+c (OH-)-c(H+) |
| A. | 配制一定物质的量浓度的溶液,向容量瓶加水至液面离刻度线1~2 cm时,改用胶头滴管定容 | |
| B. | 向某溶液中先加入Ba(NO3)2溶液,再加入足量的HNO3溶液,产生白色沉淀,则该溶液中一定含有SO42- | |
| C. | 分液操作时,将下层液体先放出,然后关闭旋塞,将上层液体从上口倒出 | |
| D. | 将油脂与氢氧化钠溶液混合充分反应后,再加入热的饱和食盐水,则可析出肥皂的主要成分 |
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量红棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品.
(1)H2SO4溶解A12O3的化学方程式是Al2O3+3H2SO4=2Al2(SO4)3+3H2O.
(2)KMnO4氧化Fe2+的离子方程式补充完整:
1MnO4-+5Fe2++8H+═1Mn2++5Fe3++4H2O
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀.
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2.
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnSO4的目的是除去过量的MnO4-.
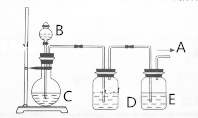
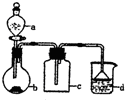 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是| 选项 | A中的物质 | b中的物质 | c中的物质 | d中的物质 |
| A | 浓氨水 | NaOH | NH3 | H2O |
| B | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
| C | 稀硝酸 | Cu | NO | H2O |
| D | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 甲烷的燃烧热为890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)$?_{500℃、30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 向Na2CO3溶液中滴入酚酞溶液,溶液变红:CO32-+2H2O?H2CO3+2OH- | |
| D. | 纯水的电离方程式:H2O+H2O?H3O++OH- |