题目内容
一定条件下,在体积为10L的密闭容器中,1mol A和1mol B进行反应:2A(g)+B(g)═2C(g),达到平衡时生成0.6mol C.下列说法正确的是( )
分析:A、依据反应平衡标志实质是变量不变分析判断;
B、反应前后气体体积减小,体积缩小浓度增大,压强增大,平衡正向进行;
C、增大压强平衡正向进行;
D、依据三段式计算C体积分数;
B、反应前后气体体积减小,体积缩小浓度增大,压强增大,平衡正向进行;
C、增大压强平衡正向进行;
D、依据三段式计算C体积分数;
解答:解:依据化学平衡三段式列式计算
2A(g)+B(g)═2C(g)
起始量(mol) 1 1 0
变化量(mol)0.6 0.3 0.6
平衡量(mol)0.4 0.7 0.6
A、反应前后都是气体,密闭容器中气体质量不变,气体体积不变,反应过程中和平衡状态下密度不变,不能判断反应达到平衡,故A错误;
B、其他条件不变,将容器体积变为5L,C的浓度变为原来的2倍,但反应前后气体体积变化,缩小体积压强增大,平衡正向进行,C的平衡浓度变化大于原来的2倍,故B错误;
C、其他条件不变,若增大压强,平衡正向进行,则物质A的转化率增大,故C错误;
D、达到平衡时,C的体积百分含量=
=0.353,故D正确;
故选D.
2A(g)+B(g)═2C(g)
起始量(mol) 1 1 0
变化量(mol)0.6 0.3 0.6
平衡量(mol)0.4 0.7 0.6
A、反应前后都是气体,密闭容器中气体质量不变,气体体积不变,反应过程中和平衡状态下密度不变,不能判断反应达到平衡,故A错误;
B、其他条件不变,将容器体积变为5L,C的浓度变为原来的2倍,但反应前后气体体积变化,缩小体积压强增大,平衡正向进行,C的平衡浓度变化大于原来的2倍,故B错误;
C、其他条件不变,若增大压强,平衡正向进行,则物质A的转化率增大,故C错误;
D、达到平衡时,C的体积百分含量=
| 0.6mol |
| 2mol-0.3mol |
故选D.
点评:本题考查化学平衡的计算应用,转化率、平衡影响因素分析判断,掌握基础是解题关键,题目难度中等.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g)根据题意完成下列各题:
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g)根据题意完成下列各题: 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g),下列有关说法正确的是( )
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g),下列有关说法正确的是( )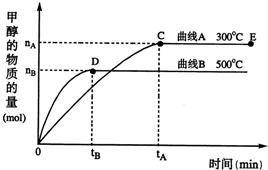 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):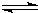 CH3OH(g)
CH3OH(g)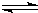 2Cu+CO2
2Cu+CO2
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO).根据题意完成下列各题:
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO).根据题意完成下列各题: