题目内容
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO).根据题意完成下列各题:
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO).根据题意完成下列各题:(1)反应达到平衡时,平衡常数表达式K=
| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
减小
减小
(填“增大”“减小”或“不变”).(2)500℃时,从反应开始到平衡,氢气的平均反应速率v(H2)=
| 2nB |
| 3tB |
| 2nB |
| 3tB |
(3)在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的
| 1 |
| 2 |
BC
BC
(填写字母).A.氢气的浓度减少
B.正反应速率加快,逆反应速率也加快
C.甲醇的物质的量增加
D.重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:
Cu2O+CO?2Cu+CO2
Cu2O+CO?2Cu+CO2
(用化学方程式表示).分析:(1)依据平衡常数概念列式,生成物平衡浓度的幂次方乘积除以生成物平衡浓度的幂次方乘积,依据图象分析温度越高平衡逆向进行,反应是放热反应分析;
(2)图象分析500°C,从反应开始到平衡,在tB时间段内甲醇增加物质的量为nB,依据化学方程式计算消耗氢气物质的量为2nB,结合速率概念计算得到;
(3)依据平衡可知2H2+CO=CH3OH,体积压缩压强增大,分析判断选项;
(4)一氧化碳和氧化亚铜反应生成铜和二氧化碳,二氧化碳抑制反应正向进行,有利于维持催化剂Cu2O的量不变.
(2)图象分析500°C,从反应开始到平衡,在tB时间段内甲醇增加物质的量为nB,依据化学方程式计算消耗氢气物质的量为2nB,结合速率概念计算得到;
(3)依据平衡可知2H2+CO=CH3OH,体积压缩压强增大,分析判断选项;
(4)一氧化碳和氧化亚铜反应生成铜和二氧化碳,二氧化碳抑制反应正向进行,有利于维持催化剂Cu2O的量不变.
解答:解:(1)依据化学反应的方程式2H2+CO=CH3OH,平衡常数K=
;图象分析温度越高,甲醇浓度减小,说明平衡逆向进行,逆向是吸热反应,正向是放热反应,升高温度平衡逆向进行,K值减小,
故答案为:
;减小;
(2)图象分析500°C,从反应开始到平衡,在tB时间段内甲醇增加物质的量为nB,依据化学方程式计算消耗氢气物质的量为2nB,氢气的反应速率=
=
mol/(L?min),故答案为:
mol/(L?min);
(3)其他条件不变的情况下,将处于E点的体系的体积压缩到原来的
,压强增大,平衡正向进行;
A.平衡正向进行,氢气物质的量减小,但体积减小为用原来的一半,氢气的浓度增大,故A错误;
B.压缩体积,增大压强,正反应速率加快,逆反应速率也加快,故B正确;
C.平衡正向进行,甲醇的物质的量增大,故C正确;
D.平衡正向进行,重新平衡时n(H2)/n(CH3OH)减小,故D错误;
故答案为:BC;
(4)反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,氧化碳和氧化亚铜反应生成铜和二氧化碳,二氧化碳抑制反应正向进行,有利于维持催化剂Cu2O的量不变,
故答案为:Cu2O+CO?2Cu+CO2.
| c(CH3OH) |
| c(CO)c2(H2) |
故答案为:
| c(CH3OH) |
| c(CO)c2(H2) |
(2)图象分析500°C,从反应开始到平衡,在tB时间段内甲醇增加物质的量为nB,依据化学方程式计算消耗氢气物质的量为2nB,氢气的反应速率=
| ||
| tB |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
(3)其他条件不变的情况下,将处于E点的体系的体积压缩到原来的
| 1 |
| 2 |
A.平衡正向进行,氢气物质的量减小,但体积减小为用原来的一半,氢气的浓度增大,故A错误;
B.压缩体积,增大压强,正反应速率加快,逆反应速率也加快,故B正确;
C.平衡正向进行,甲醇的物质的量增大,故C正确;
D.平衡正向进行,重新平衡时n(H2)/n(CH3OH)减小,故D错误;
故答案为:BC;
(4)反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,氧化碳和氧化亚铜反应生成铜和二氧化碳,二氧化碳抑制反应正向进行,有利于维持催化剂Cu2O的量不变,
故答案为:Cu2O+CO?2Cu+CO2.
点评:本题考查平衡常数的分析应用,图象分析判断反应特征,平衡影响因素的分析理解,掌握基础是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g)根据题意完成下列各题:
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g)根据题意完成下列各题: 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g),下列有关说法正确的是( )
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g),下列有关说法正确的是( )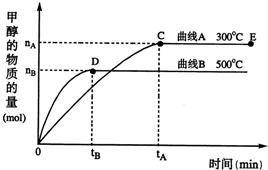 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):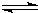 CH3OH(g)
CH3OH(g)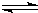 2Cu+CO2
2Cu+CO2