题目内容
1.下列晶胞所对应的化学式正确的是( )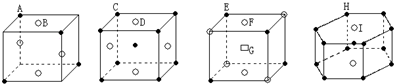
| A. | A3B4 | B. | CD | C. | EF3G2 | D. | H5I |
分析 根据均摊法可知,位于立方体晶胞顶点上的原子有$\frac{1}{8}$属于该晶胞,位于立方体晶胞棱边上的原子有$\frac{1}{4}$属于该晶胞,位于立方体晶胞面心上的原子有$\frac{1}{2}$属于该晶胞,位于立方体晶胞体心上的全部属于该晶胞,位于六棱柱晶胞中顶点上的原子有$\frac{1}{6}$属于该晶胞,位于六棱柱晶胞面心上的原子有$\frac{1}{2}$属于该晶胞,位于六棱柱晶胞体心上的全部属于该晶胞,据此分析;
解答 解:A、在第一个晶胞结构中,含有A原子数为4×$\frac{1}{8}$=$\frac{1}{2}$,含有B原子数为4×$\frac{1}{2}$=2,所以化学式为AB4,故A错误;
B、在第二个晶胞结构中,含有C原子数为8×$\frac{1}{8}$+1=2,含有D原子数为4×$\frac{1}{2}$=2,所以化学式为CD,故B正确;
C、在第三个晶胞结构中,含有E原子数为4×$\frac{1}{8}$=$\frac{1}{2}$,含有F原子数为4×$\frac{1}{8}$+2×$\frac{1}{2}$=$\frac{3}{2}$,含有G原子数为1,所以化学式为EF3G2,故C正确;
D、在第四个晶胞结构中,含有H原子数为12×$\frac{1}{6}$+1=3,含有I原子数为2×$\frac{1}{2}$=1,所以化学式为H3I,故D错误;
故选:BC.
点评 本题主要就考查了均摊法计算晶胞的化学式,题目难度不大,能理解均摊法即可解决问题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.有关铁的化合物的说法中,错误的是( )
| A. | FeO不稳定,在空气中加热迅速被氧化成Fe2O3 | |
| B. | 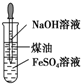 由图示操作可制取Fe(OH)2 | |
| C. | Fe3O4、Fe(OH)3都可以由化合反应制得 | |
| D. | Fe(OH)3胶体呈红褐色、透明,能发生丁达尔现象 |
9.向含有Fe2+,Al3+,NH4+,Na+,Fe3+的溶液中加入过量的Na2O2固体,微热溶液使其充分反应,再通入过量的HCl气体,则反应后溶液中离子浓度增加的是( )
| A. | Na+和Fe2+ | B. | Al3+和Na+ | C. | Fe2+和NH4+ | D. | Fe3+和Na+ |
16.化学与材料科学息息相关,从一定意义上讲,材料是科学技术的先导,没有新材料的发展,就不可能使新的科学技术成为生产力.下列有关材料的说法不正确的是( )
| A. | 材料是为人类社会所需要并能用于制造有用器物的物质 | |
| B. | 人类使用和制造材料有悠久的历史,制造出的第一种材料是陶 | |
| C. | 体型结构的酚醛树脂制成的塑料,加工成型后,受热熔化后还可以制成其它形状的器物 | |
| D. | 高分子分离膜是具有传统高分子材料的机械性能,又具有特殊分离功能的功能高分子材料制成的薄膜 |
13.把pH=13的NaOH溶液与pH=2的硫酸溶液混合后,所得溶液的pH=11,则NaOH溶液和硫酸溶液的体积之比为( )
| A. | 1:1 | B. | 1:5 | C. | 1:9 | D. | 2:3 |
10.维生素C具有的性质是( )
| A. | 难溶于水 | B. | 易溶于水 | C. | 弱还原性 | D. | 强氧化性 |
7.下列各组物质中,属于同素异形体的是( )
| A. | 红磷和白磷 | B. | 冰和干冰 | C. | NH3和NH4+ | D. | O2和O2- |
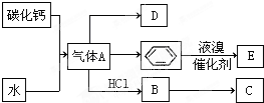
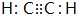 ;D的空间构型为平面结构,键角为120°;
;D的空间构型为平面结构,键角为120°; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反应类型为取代反应.
+HBr,其反应类型为取代反应.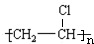 ,其反应类型为加聚反应.
,其反应类型为加聚反应.