题目内容
2.下列实验装置或实验方案能达到目的是( )| A. | 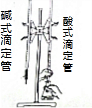 用HF标准溶液测定未知浓度的NaOH溶液 用HF标准溶液测定未知浓度的NaOH溶液 | |
| B. | 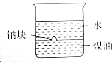 验证密度:ρ(水)<ρ(钠)<ρ(煤油) 验证密度:ρ(水)<ρ(钠)<ρ(煤油) | |
| C. | 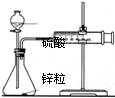 测定锌与硫酸反应的速率 测定锌与硫酸反应的速率 | |
| D. | 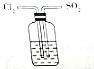 验证SO2和Cl2等物质的量混合增强漂白效果 验证SO2和Cl2等物质的量混合增强漂白效果 |
分析 A.用HF标准液测定未知浓度的NaOH溶液,HF溶液需要盛放在酸式滴定管中;
B.密度ρ(水)>ρ(钠)>ρ(煤油);
C.测定锌与硫酸反应的速率还需要测定时间的仪器;
D.SO2和Cl2等物质的量通入水中发生反应Cl2+2H2O+SO2=H2SO4+2HCl,硫酸和盐酸都没有漂白性.
解答 解:A.用HF标准液测定未知浓度的NaOH溶液,HF溶液呈酸性,需要盛放在酸式滴定管中,故A正确;
B.水和煤油不互溶,所以二者会分层,但密度:ρ(水)>ρ(煤油),所以水在下方、煤油在上方,Na密度介于二者之间,钠和水剧烈反应生成NaOH和氢气,和煤油不反应,钠会沉在煤油中但会浮在水面上,钠和水反应产生的气体将钠推到煤油中,钠在煤油中下沉到达水和煤油交界处,则钠就在水和煤油中往复运动,该实验证明密度ρ(水)>ρ(钠)>ρ(煤油),故B错误;
C.测定锌与硫酸反应的速率还需要测定时间的仪器秒表,所以不能实现实验目的,故C错误;
D.SO2和Cl2等物质的量通入水中发生反应Cl2+2H2O+SO2=H2SO4+2HCl,硫酸和盐酸都没有漂白性,所以二者等物质的量通入水中后溶液没有漂白性,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及基本操作、物质性质等知识点,明确实验原理及基本操作方法是解本题关键,注意操作规范性、物质性质,易错选项是D.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
13.把pH=13的NaOH溶液与pH=2的硫酸溶液混合后,所得溶液的pH=11,则NaOH溶液和硫酸溶液的体积之比为( )
| A. | 1:1 | B. | 1:5 | C. | 1:9 | D. | 2:3 |
10.维生素C具有的性质是( )
| A. | 难溶于水 | B. | 易溶于水 | C. | 弱还原性 | D. | 强氧化性 |
17.下列说法中正确的是( )
| A. | 用电解法精炼铜时粗铜作阴极 | |
| B. | 在其他条件不变时,增大压强一定会破坏气体反应的平衡状态 | |
| C. | 化学平衡常数K只与温度有关,与反应物浓度、体系的压强无关 | |
| D. | 需要加热的化学反应都是吸热反应 |
3.常温pH=12的强碱溶液与pH=1的强酸溶液混合,所得混合液的pH=7,则强碱与强酸的体积比是( )
| A. | 11:1 | B. | 10:1 | C. | 9:1 | D. | 1:1 |
10.用如图所示装置进行实验.能形成‘喷泉”的气体是( )
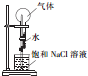

| A. | O2 | B. | Cl2 | C. | HCl | D. | N2 |
7.下列各组物质中,属于同素异形体的是( )
| A. | 红磷和白磷 | B. | 冰和干冰 | C. | NH3和NH4+ | D. | O2和O2- |
8.铂金色泽淡雅而华贵,象征着纯洁与高尚,近年来铂金饰品越来越受到人们宠爱.我国科学家在世界上首次发现铂的一种新核素${\;}_{78}^{202}$Pt,下列说法正确的是( )
| A. | ${\;}_{78}^{202}$Pt原子核中含有78个中子 | |
| B. | ${\;}_{78}^{202}$Pt原子核外有124个电子 | |
| C. | ${\;}_{78}^{195}$Pt和${\;}_{78}^{202}$Pt互为同素异形体 | |
| D. | ${\;}_{78}^{195}$Pt和${\;}_{78}^{202}$Pt互为同位素 |