题目内容
7.在密闭容器中发生下列反应aA(g)?cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的2.1倍,下列叙述不正确的是( )| A. | A的转化率变大 | B. | a<c+d | ||
| C. | A的质量分数变小 | D. | 平衡向正反应方向移动 |
分析 将气体体积压缩到原来的一半,若平衡不移动,C的浓度为原来的2倍,而当再次达到平衡时,C的浓度为原平衡的2.1倍,可知增大压强,平衡正向移动,以此来解答.
解答 解:由上述分析可知,增大压强,平衡正向移动,则
A.平衡正向移动,A的转化率变大,故A正确;
B.平衡正向移动,则a>c+d,故B错误;
C.平衡正向移动,A的质量分数变小,故C正确;
D.由分析可知平衡向正反应方向移动,故D正确;
故选B.
点评 本题考查化学平衡移动,为高频考点,把握体积与压强的关系、压强对平衡移动的影响为解答本题的关键,侧重分析与应用能力的考查,注意平衡移动方向的判断,题目难度不大.

练习册系列答案
相关题目
8.“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
| A. | 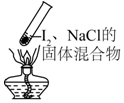 加热时,上部汇聚了固体碘,说明碘的热稳定性较差 | |
| B. | 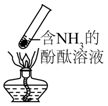 加热时,中部溶液变红,冷却后又变为无色 | |
| C. | 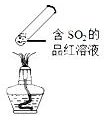 加热时,中部溶液变红,冷却后又变为无色 | |
| D. |  \加热时,上部汇聚了白色固体,说明氯化铵易升华 |
9.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 28 g氮气含有的原子数为NA | |
| B. | 标准状况下,22.4 L水中含有的水分子数为NA | |
| C. | 1 molOH-含有的电子数为10NA | |
| D. | 0.1 L 1 mol•L-1NaCl溶液中含有Na+个数为NA |
2.下列化学术语或表示方法错误的是( )
| A. | 乙烯的结构简式为:CH2=CH2 | |
| B. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| C. | 醋酸的分子式:CH3COOH | |
| D. | 乙醇的结构式为: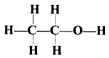 |
12.由乙醇及必要的无机试剂合成乙二醇,其依次发生的反应类型为( )
| A. | 取代,消去,加成 | B. | 加成,消去,取代 | C. | 消去,加成,取代 | D. | 取代,加成,消去 |
19.当氯气用于漂白时,真正起漂白作用的是( )
| A. | Cl- | B. | HClO | C. | HCl | D. | Cl2 |
17.除去MgO中的Al2O3可选用的试剂是( )
| A. | NaOH溶液 | B. | 氨水 | C. | 稀盐酸 | D. | CO气体 |
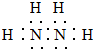 ,HCN中C的化合价为-2.
,HCN中C的化合价为-2.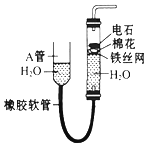 如图中的实验装置可用于制取乙炔.请填空:
如图中的实验装置可用于制取乙炔.请填空: