题目内容
10.下列化合物中含有2个手性碳原子的是( )| A. |  | B. |  | C. |  | D. | 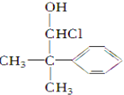 |
分析 手性碳原子指连有四个不同基团的碳原子,手性碳原子判断注意:1、手性碳原子一定是饱和碳原子;2、手性碳原子所连接的四个基团要是不同的.
解答 解:A、 只有如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有1个手性碳原子,故A不符合;
只有如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有1个手性碳原子,故A不符合;
B、 如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有2个手性碳原子,故B符合;
如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有2个手性碳原子,故B符合;
C、 只有如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有1个手性碳原子,故C不符合;
只有如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有1个手性碳原子,故C不符合;
D、 只有如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有1个手性碳原子,故D不符合.
只有如图标记“*”的碳原子连接四个不同的基团,是手性碳原子,含有1个手性碳原子,故D不符合.
故选:B.
点评 本题考查手性碳原子的判断,比较基础,手性碳原子判断注意:1、手性碳原子一定是饱和碳原子;2、手性碳原子所连接的四个基团要是不同的.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
20.下列各组表述中,两个微粒属于同种元素原子的是( )
| A. | M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2 的原子 | |
| B. | 2p能级有一个未成对电子的基态原子和原子的价电子排布为2s22p5 | |
| C. | 3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2 | |
| D. | 最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p1的原子 |
1.下列实验装置正确的是( )
| A. |  实验室制乙烯 | B. |  酯化反应 | ||
| C. |  实验室制取Cl2 | D. |  中和热的测定 |
18.正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.

发生的反应如下:
CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据如下:
实验步骤如下:
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.
②在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分.
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.
回答下列问题:
(1)B仪器的名称是滴液漏斗,D仪器的名称是直形冷凝管.
(2)沸石的作用是防止暴沸.
(3)将正丁醛粗产品置于分液漏斗中分液时,水在下层(填“上”或“下”)
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)本实验中,正丁醛的产率为51%.

发生的反应如下:
CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据如下:
| 沸点/℃ | 密度(g.cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.5 | 0.8107 | 微溶 |
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.
②在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分.
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.
回答下列问题:
(1)B仪器的名称是滴液漏斗,D仪器的名称是直形冷凝管.
(2)沸石的作用是防止暴沸.
(3)将正丁醛粗产品置于分液漏斗中分液时,水在下层(填“上”或“下”)
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)本实验中,正丁醛的产率为51%.
5.下列关于σ键和π键的理解不正确的是( )
| A. | 共价单键都是σ键,共价双键中有一个σ键和一个π键 | |
| B. | σ键可以绕键轴旋转,π键一定不能绕键轴旋转 | |
| C. | H2 分子中的σ键是s-s σ键,HClO分子中的σ键是p-p σ键 | |
| D. | C2H4分子中有5个σ键和一个π键,N2H4中只有5个σ键 |
15.现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤 形,A与氢元素形成化合物AH5除了配位键外还有离子键和极性键.
(2)某同学根据上述信息,所画的C电子排布图如图违背了泡利 原理.
(3)DE3 中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形.检验F元素的方法是焰色反应.
(4)A2与B22+互为等电子体,B22+的电子式可表示为 ;1mol B22+中含有的π键数目为2NA.
;1mol B22+中含有的π键数目为2NA.
(5)下列电子云图象均为成键后电子云图象,其中可表示一个E原子与一个E原子的是E,表示一个氢原子与一个E原子的是D.

| A.元素原子的核外p电子总数比s电子总数少1 |
| B.元素价电子排布式为nsnnp2n |
| C.元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| D.原子核外所有p轨道全满或半满 |
| E.元素的主族序数与周期数的差为4 |
| F.是前四周期中电负性最小的元素 |
(2)某同学根据上述信息,所画的C电子排布图如图违背了泡利 原理.

(3)DE3 中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形.检验F元素的方法是焰色反应.
(4)A2与B22+互为等电子体,B22+的电子式可表示为
 ;1mol B22+中含有的π键数目为2NA.
;1mol B22+中含有的π键数目为2NA.(5)下列电子云图象均为成键后电子云图象,其中可表示一个E原子与一个E原子的是E,表示一个氢原子与一个E原子的是D.

2.“神州八号”飞船成功发射升空之后,完成了与1个月前发射的“天宫一号”的成功交会对接,其中新材料铝锂合金为“太空之吻”提供了保障.下列关于铝锂合金的认识正确的( )
| A. | 铝锂合金是铝与锂形成的一种化合物 | |
| B. | 锂是碱金属元素,性质活泼,铝锂合金与水反应生成氢气 | |
| C. | 铝离子和锂离子的核外电子排布相同 | |
| D. | 若铝锂合金中锂含量为1.1%,则127.3g铝锂合金中含有锂原子0.2mol |