题目内容
8.分子树(Dendrimers)是指分子中有树状结构的高度支化大分子,这类大分子的制备方法之一就是Michael加成反应.反应的一个简单例子如下:(C2H5)2NH+H2C=CHCO2Et$→_{0℃}^{惰性溶剂+醋酸}$(C2H5)2N-CH2CH2CO2Et(注:Et为乙基),一个分子树可通过下列反应得到:
①NH3用过量的丙烯睛(H2C=CHCN)处理得到含有3个氰基的产物
②上述所得产物在催化剂作用下用H2催化还原,得到一种带有三个伯胺(-NH2)的产物.
③这种初级伯胺产物再用过量的丙烯腈处理.
④步骤③的产物再在催化剂作用下用H2氢化,得到六胺化合物.这就是一种支化大分子的开始.
(1)(a)步骤①的反应方程式NH3+3H2C=CHCN→N(CH2CH2CN)3;
(b)步骤②的反应方程式N(CH2CH2CN)3+6H2→N(CH2CH2CH2NH2)3;
(c)步骤④氢化得到的反应产物的结构简式N[CH2CH2CH2N(CH2CH2CH2NH2)2]3.
用丙烯腈处理的结果和氨基的还原结果可以重复几次,最终形成带有伯胺基团的球形分子(-NH2已位于表面).
(2)计算经5次全循环(第一次循环由步骤①+②组成)后,在分子树上有48个末端基.
(3)(a)每摩尔NH3,进行5次循环时,共需丙烯腈的物质的量为93mol.
(b)分子树每经一次循环分子直径增加约1nm.计算5次循环后分子树的体积6.54×10-26m3.
分析 (1)(a)步骤①NH3用过量的丙烯睛(H2C=CHCN)处理得到含有3个氰基的产物,发生的是加成反应,NH3中的每一个N-H断开加成H2C=CHCN中的碳碳双键,H2C=CHCN的双键断开,方程式为:NH3+3H2C=CHCN→N(CH2CH2CN)3;
(b)步骤②含有3个氰基的产物在催化剂作用下用H2催化还原,得到一种带有三个伯胺(-NH2)的产物,也就是一个N(CH2CH2CN)3中的三个-C≡N键断裂,被氢气氢化,得到三个-NH2.方程式为:N(CH2CH2CN)3+6H2→N(CH2CH2CH2NH2)3;
(c)N(CH2CH2CH2NH2)3 分子中含6个氢原子,需要和6个丙烯睛(H2C=CHCN)加成反应得到N[CH2CH2CH2N(CH2CH2CN)2]3,再氢化需要12个氢气加成得到反应产物的结构简式N[CH2CH2CH2N(CH2CH2CH2NH2)2]3,如此循环往复;
(2)经5次全循环(第一次循环由步骤①+②组成)后,依据结构特征分析计算在分子树上含有的末端基数目;
(3)1个分子的直径近似为10-10m,分子树每经一次循环分子直径增加约1nm,每摩尔NH3,进行5次循环时,分子直径为6×10-10m,最终形成带有伯胺基团的球形分子,分子的体积V=$\frac{4}{3}$πr3计算得到;
解答 解:(1)(a)步骤①NH3用过量的丙烯睛(H2C=CHCN)处理得到含有3个氰基的产物,发生的是加成反应,NH3中的每一个N-H断开加成H2C=CHCN中的碳碳双键,H2C=CHCN的双键断开,方程式为:NH3+3H2C=CHCN→N(CH2CH2CN)3,
故答案为:NH3+3H2C=CHCN→N(CH2CH2CN)3 ;
(b)步骤②含有3个氰基的产物在催化剂作用下用H2催化还原,得到一种带有三个伯胺(-NH2)的产物,也就是一个N(CH2CH2CN)3中的三个-C≡N键断裂,被氢气氢化,得到三个-NH2.方程式为:N(CH2CH2CN)3+6H2→N(CH2CH2CH2NH2)3,
故答案为:N(CH2CH2CN)3+6H2→N(CH2CH2CH2NH2)3;
(c)步骤③的产物再在催化剂作用下用H2氢化,得到六胺化合物,N(CH2CH2CH2NH2)3 分子中含6个氢原子,需要和6个丙烯睛(H2C=CHCN)加成反应得到N[CH2CH2CH2N(CH2CH2CN)2]3,再氢化需要12个氢气加成得到反应产物的结构简式N[CH2CH2CH2N(CH2CH2CH2NH2)2]3,如此循环往复,
故答案为:N[CH2CH2CH2N(CH2CH2CH2NH2)2]3;
(2)第一次循环为由步骤①+②组成,反应为NH3+3H2C=CHCN→N(CH2CH2CN)3 ,N(CH2CH2CN)3+6H2→N(CH2CH2CH2NH2)3,得到产物中每1mol含氨基为3mol,第二此循环是得到六胺化合物,N(CH2CH2CH2NH2)3 分子中含6个氢原子,需要和6个丙烯睛(H2C=CHCN)加成反应得到N[CH2CH2CH2N(CH2CH2CN)2]3,末端基氨基为6mol,第三个循环氢化需要12个氢气加成得到反应产物的结构简式N[CH2CH2CH2N(CH2CH2CH2NH2)2]3,末端基为氨基为12mol,第四次循环则为产物与12mol丙烯睛(H2C=CHCN)加成反应,得到氨基24mol,第五次循环得到氨基氢48mol,
故答案为:48;
(3)(a)依据(2)分析把过程中需要的丙烯睛相加得到需要的丙烯睛个数=3+6+12+24+48=93,
故答案为:93;
(b)1个分子的直径近似为10-10m,分子树每经一次循环分子直径增加约1nm,每摩尔NH3,进行5次循环后,分子直径为5.0×10-9m,最终形成带有伯胺基团的球形分子,分子的体积V=$\frac{4}{3}$πr3=$\frac{4}{3}$×3.14×($\frac{5}{2}$)3=6.54×10-26m3;
故答案为:6.54×10-26m3;
点评 不本题考查了物质制备的过程分析,有机物结构的变化和反应实质理解应用,规律的归纳整理是解题关键,题目难度较大.

 名校课堂系列答案
名校课堂系列答案| A. | 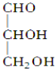 | B. | 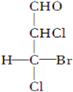 | C. | 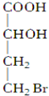 | D. | 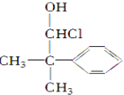 |
| A. | 碳的燃烧 | B. | 葡萄糖在人体内氧化分解 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 锌粒与稀H2SO4反应制取H2 |
| A. | 分离苯和水的混合物,可用分液法 | |
| B. | 从Na2CO3溶液中得到Na2C03,可用过滤法 | |
| C. | 分离酒精和CCl4的混合物,可用分液法 | |
| D. | 分离NaCl和AgCl的混合物,可用萃取法 |
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s | 0 | 500 | 100 0 | 150 0 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 | |
| B. | 500s内N2O5分解速率为2.96×10-3mol•L-1•s-1 | |
| C. | 达平衡后其他条件不变,将容器的体积压缩到原来的 $\frac{1}{2}$,则c(N2O5)>5.00mol•L-1 | |
| D. | T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50% |
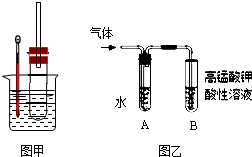 Ⅰ.某学习小组用乙醇与氢溴酸为原料制备溴乙烷.
Ⅰ.某学习小组用乙醇与氢溴酸为原料制备溴乙烷.