题目内容
对于反应:N2+O2?2NO,在密闭容器中进行,下列条件能加快反应速率的是( )
| A、缩小体积使压强增大 |
| B、降低体系温度 |
| C、体积不变充入He使气体压强增大 |
| D、保持总压强不变,充入Ne气体 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:影响化学反应速率快慢的因素有内因和外因,反应物本身的性质(内因),温度、浓度、压强、催化剂等为影响化学反应速率的外界因素,对于反应N2+O2?2NO是一个反应前后体积不变的反应,以此解答该题.
解答:
解:A.缩小体积,反应物的浓度增大,活化分子的数目增多,能使反应速率增大,故A正确;
B.降低温度,反应速率减慢,故B错误;
C.体积不变,充入He,反应物的浓度不变,反应速率不变,故C错误;
D.若使总压强不变充入He,反应体系的压强减小,反应速率减慢,故D错误.
故选A.
B.降低温度,反应速率减慢,故B错误;
C.体积不变,充入He,反应物的浓度不变,反应速率不变,故C错误;
D.若使总压强不变充入He,反应体系的压强减小,反应速率减慢,故D错误.
故选A.
点评:本题考查影响化学反应速率的外界因素的适用范围,为高频考点,明确温度、压强、浓度、催化剂等常见的对反应的影响因素是解答的关键,题目较简单.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
下列说法中正确的是( )
①钠在空气中燃烧生成淡黄色的Na2O2;
②酸雨是pH<7的雨水;
③铝 铁 铜,三者对应的氧化物均为碱性氧化物;
④金属钠着火时用细沙子扑灭;
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性.
①钠在空气中燃烧生成淡黄色的Na2O2;
②酸雨是pH<7的雨水;
③铝 铁 铜,三者对应的氧化物均为碱性氧化物;
④金属钠着火时用细沙子扑灭;
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性.
| A、②③ | B、①②③ |
| C、①④ | D、①②③⑤ |
下列说法正确的是( )
| A、25℃时、用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH |
| B、饱和小苏打溶液中:c(Na+)=c(HCO3-) |
| C、Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解程度减小,溶液的pH 减小 |
| D、室温下,对于0.10 mol?L-1的氨水,用HNO3溶液完全中和后,溶液不显中性 |
具有相同数目氧原子的SO2和SO3,下列关系中一定正确的是( )
| A、n(SO2):n(SO3)=2:3 |
| B、V(SO2):V(SO3)=3:2 |
| C、m(SO2):m(SO3)=6:5 |
| D、Mr(SO2):Mr(SO3)=5:4 |
溶于水后溶液呈酸性的物质是( )
| A、过氧化钠 | B、生石灰 |
| C、二氧化硫 | D、小苏打 |


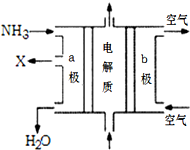 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题: