题目内容
1.下列说法正确的是( )| A. | 在测定中和热的实验中,为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 | |
| B. | 酸碱中和滴定实验中,锥形瓶要用待装液预先润洗 | |
| C. | 在测定中和热的实验中,用0.5mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 | |
| D. | 测溶液PH值时,PH试纸不能润湿 |
分析 A.测定溶液温度,温度计不能接触烧杯底部;
B.锥形瓶要用待装液预先润洗,导致消耗的标准液体积偏大;
C.弱电解质电离需要吸收热量;
D.试纸润湿相当于将待测液稀释.
解答 解:A.温度计水银球测烧杯内的热水的温度,不能接触烧杯底部接触烧杯底部,故A错误;
B.锥形瓶要用待装液预先润洗,导致消耗的标准液体积偏大,所测标准液浓度偏高,故B错误;
C.在测定中和热的实验中,用0.5mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值不相同,用醋酸溶液测得的数值小于用盐酸测得的数值,故C错误;
D.测溶液PH值时,PH试纸润湿,相当于将待测液稀释,测定pH值可能产生误差,故D正确;
故选:D.
点评 本题为实验题,涉及中和热的测定、中和滴定、pH试纸的使用,熟悉中和热测定原理、中和滴定原理及操作步骤是解题关键,题目难度不大,侧重考查学生对基础知识掌握熟练程度.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
12.在一定条件下,红棕色的NO2可以发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0,下列叙述中正确的是( )
| A. | 恒温恒容,充入NO2气体,其转化率增大 | |
| B. | 加压,平衡向逆反应方向移动,混合气体颜色变深 | |
| C. | 若平衡常数增大,则可能是升高了温度或减小了体系的压强 | |
| D. | 当2v正(NO)=v逆(O2)时,反应达到化学平衡状态 |
13.化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( )
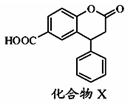

| A. | 分子中两个苯环一定处于同一平面 | |
| B. | 不能与饱和Na2CO3溶液反应 | |
| C. | 在酸性条件下水解,水解产物只有一种 | |
| D. | 1mol化合物X最多能与7molH2反应 |
10.Na2O2是中学化学常用试剂,下列说法错误是( )
| A. | 0.1mol Na2O2与足量CO2反应转移的电子的物质的量为0.1mol | |
| B. | 将Na2O2粉末加入到饱和NaOH溶液中,OH-离子浓度一定不变 | |
| C. | 等物质的量的Na2O2与Na2O溶于等质量水中得到的NaOH的物质的量浓度相同 | |
| D. | 等质量的Na2O2与Na2S晶体中含有相同数目的阴离子 |
16.甲醇是重要的化工原料,又可做燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,主要反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2=-58kJ/mol
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
已知反应①中的相关的化学键键能数据如下:
回答下列问题:
①△H3=+41kJ/mol.
②25℃,101kPa条件下,测得16g甲醇完全燃烧释放出Q kJ的热量,请写出表示甲醇燃烧热的热化学方程式CH3OH(l)+$\frac{3}{2}$O2(g)=CO2+2H2O△H=-2QkJ/mol.
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2=-58kJ/mol
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
已知反应①中的相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O (CO中的化学键) | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
①△H3=+41kJ/mol.
②25℃,101kPa条件下,测得16g甲醇完全燃烧释放出Q kJ的热量,请写出表示甲醇燃烧热的热化学方程式CH3OH(l)+$\frac{3}{2}$O2(g)=CO2+2H2O△H=-2QkJ/mol.