题目内容
10.Na2O2是中学化学常用试剂,下列说法错误是( )| A. | 0.1mol Na2O2与足量CO2反应转移的电子的物质的量为0.1mol | |
| B. | 将Na2O2粉末加入到饱和NaOH溶液中,OH-离子浓度一定不变 | |
| C. | 等物质的量的Na2O2与Na2O溶于等质量水中得到的NaOH的物质的量浓度相同 | |
| D. | 等质量的Na2O2与Na2S晶体中含有相同数目的阴离子 |
分析 A、过氧化钠与水和二氧化碳的反应是自身的氧化还原反应;
B、随着一小块Na2O2固体的投入,氢氧化钠饱和溶液中水被反应所消耗,饱和溶液析出固体溶质;由于溶液温度不变,变化后所得溶液仍为氢氧化钠的饱和溶液;
C、Na2O和Na2O2物质的量相等且由方程式易知,Na2O2放在溶液中增加的质量为Na2O2中的Na2O部分,由此可知两溶液的质量相同;
D、Na2O2与Na2S的摩尔质量相等,而且过氧化钠中含有阳离子与阴离子的数目之比为2:1.
解答 解:A、过氧化钠与水和二氧化碳的反应是自身的氧化还原反应,所以0.1mol Na2O2与足量CO2反应转移的电子的物质的量为0.1mol,故A正确;
B、随着一小块Na2O2固体的投入,氢氧化钠饱和溶液中水被反应所消耗,饱和溶液析出固体溶质;由于溶液温度不变,变化后所得溶液仍为氢氧化钠的饱和溶液,如果温度不变,氢氧根离子浓度不变,故B错误;
C、Na2O和Na2O2物质的量相等且由方程式易知,Na2O2放在溶液中增加的质量为Na2O2中的Na2O部分,由此可知两溶液的质量相同,则NaOH的物质的量浓度相同,故C正确;
D、Na2O2与Na2S的摩尔质量相等,而且过氧化钠中含有阳离子与阴离子的数目之比为2:1,所以等质量的Na2O2与Na2S晶体中含有相同数目的阴离子,故D正确;
故选B.
点评 本题考查钠的重要化合物和溶液浓度的计算,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
20.用酸式滴定管准确移取20.00mL某未知浓度的硫酸于一洁净的锥形瓶中,然后用0.20mol/L的氢氧化钠溶液(指示剂为酚酞)滴定,滴定结果如下:
(1)根据以上数据可以计算出硫酸的物质的量浓度为0.091mol/L(保留小数点后两位数字).
(2)以下操作可能造成测定结果偏低的是B(填写序号).
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.滴定管在滴定前尖嘴处有气泡,滴定后消失
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管.
| 实验编号 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.40mL |
| 第二次 | 3.00mL | 21.10mL |
| 第三次 | 0.20mL | 20.40mL |
| 第四次 | 0.00mL | 18.20mL |
(2)以下操作可能造成测定结果偏低的是B(填写序号).
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.滴定管在滴定前尖嘴处有气泡,滴定后消失
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管.
1.下列说法正确的是( )
| A. | 在测定中和热的实验中,为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 | |
| B. | 酸碱中和滴定实验中,锥形瓶要用待装液预先润洗 | |
| C. | 在测定中和热的实验中,用0.5mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 | |
| D. | 测溶液PH值时,PH试纸不能润湿 |
18.用电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变,且用惰性电极,下列说法不正确的是( )
| A. | 当电池负极消耗m g气体时,电解池阴极同时有m g气体生成 | |
| B. | 电池的正极反应式为:O2+2H2O+4e-═4OH- | |
| C. | 电池中c(KOH)不变;电解池中溶液pH变大 | |
| D. | 电解后c(Na2CO3)不变,且溶液中有Na2CO3﹒10H2O晶体析出 |
15.常温下,下列四种溶液中由电离生成的c(H+)之比(①:②:③:④)为( )
①1mol/L的盐酸; ②0.1mol/L盐酸; ③0.01mol/L的NaOH溶液; ④1mol/L的NaOH溶液.
①1mol/L的盐酸; ②0.1mol/L盐酸; ③0.01mol/L的NaOH溶液; ④1mol/L的NaOH溶液.
| A. | 1:10:100:1 | B. | 1:10-1:10-12:10-14 | ||
| C. | 14:13:12:14 | D. | 1:2:12:14 |
2.在浓度均为3mol/L的盐酸和硫酸各100mL溶液中,分别加入等质量的铁粉,充分反应后生成气体质量之比为3:4.则加入铁粉的质量是( )
| A. | 1.8 g | B. | 11.2 g | C. | 5.6 g | D. | 8.4 g |
5.T℃时,将A和B各0.32mol充入恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)△H=-a kJ•mol-1(a>0),反应过程中测定的数据如表,下列说法正确的是( )
| t/min | 0 | 2 | 4 | 7 | 9 |
| n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
| A. | 若起始时向容器中充入0.64 mol C,则达平衡时吸收的热量为0.12a kJ | |
| B. | 恒温,如果压缩容器体积,B的浓度和体积分数均不变 | |
| C. | 若起始时向容器中充入 0.64 mol A 和 0.64 mol B,则达平衡时 n(C)<0.48 mol | |
| D. | 恒温、恒容,向平衡体系中再充入0.32 mol A,再次平衡时,B的转化率增大 |
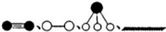 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用图1表示:
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用图1表示: