题目内容
5.下列有关物质的性质与应用不相对应的是( )| A. | 氢氟酸易与SiO2反应,可用于刻蚀玻璃 | |
| B. | Al和Fe2O3能发生铝热反应,可用于焊接钢轨 | |
| C. | NH3具有碱性,可用NH3与灼热的CuO作用制取少量N2 | |
| D. | Fe具有良好的导电性,可用Fe作电解食盐水的阴极材料 |
分析 A、氢氟酸属于弱酸,能与二氧化硅反应;
B、铝热反应是放热反应;
C、NH3具有还原性;
D、Fe具有良好导电性,可以做电极,而且活泼只用作阴极.
解答 解:A、玻璃中含有二氧化硅,虽然氢氟酸是弱酸,但氢氟酸和二氧化硅反应生成四氟化硅和水,所以氢氟酸可用于刻蚀玻璃,故A正确;
B、铝热反应是放热反应,所以可以用于焊接钢轨,故B正确;
C、NH3具有还原性,可用NH3与灼热的CuO发生氧化还原反应制取少量氮气,故C错误;
D、Fe具有良好导电性,可以做电极,而且活泼只用作阴极,故D正确;
故选C.
点评 本题考查了物质的性质和用途,明确性质决定用途、用途体现性质是解本题关键,难度不大.

练习册系列答案
相关题目
15.黑火药是我国古代四大发明之一,配方为‘一硫二硝三木炭”,下列说法中不正确的是( )
| A. | 硝是指硝酸 | B. | 黑火药爆炸是氧化还原反应 | ||
| C. | 木炭在反应中做还原剂 | D. | 反应放热并产生大量气体 |
13.设NA为阿伏加德罗常数的值.下列说法中正确的是( )
| A. | 在密闭容器中加入1mol N2和3mol H2,充分反应生成NH3分子数为2NA | |
| B. | 0.1mol-NH2(氨基)中含有的电子数为0.7NA | |
| C. | 30g SiO2中含有的Si-O键数目为2NA | |
| D. | 标准状况下,4.48 L N2所含的共用电子对数0.2NA |
20.用NA表示阿佛加德罗常数的值,下列说法中正确的是( )
| A. | 1mol甲烷的质量与NA个甲烷分子的质量之和相等 | |
| B. | 28g氮气与40g氩气所含的原子数目相等,都是NA个 | |
| C. | 2.3g钠由原子变成离子,失去的电子数为0.1个 | |
| D. | 18g重水(D2O)所含的电子数为10NA |
17.将一定量的Cl2通入体积为40mL、浓度为7.5mol/L的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),测得反应后溶液中有三种含氯元素的离子,其中ClO-物质的量为0.06mol和ClO3-物质的量0.03mol,下列说法不正确的是( )
| A. | 该反应的离子方程式为:5Cl2+10 OH-═7Cl-+2ClO-+ClO3-+5H2O | |
| B. | 该反应中,氧化剂与还原剂物质的量之比为5:3 | |
| C. | 上述苛性钾溶液中含有0.3mol的KOH | |
| D. | 反应后生成的ClO-和 ClO3- 两种离子在一定条件下均有氧化性 |
5.化学与生活密切相关,下列生活中常见物质的俗名与化学式相对应的是( )
| A. | 食醋-C2H5OH | B. | 明矾-KAl(SO4)2 | C. | 苏打-NaHCO3 | D. | 生石灰-CaO |
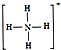 ,白磷(P4)的结构式为
,白磷(P4)的结构式为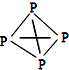 ,请画出N4H44+的结构式
,请画出N4H44+的结构式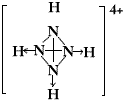 .
.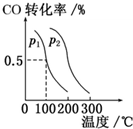 联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.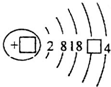 ,请补充完整:
,请补充完整: