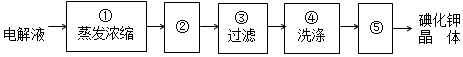
题目内容
4.在光照条件下,将等物质的量的甲烷和氯气混合,充分反应后,得到产物的物质的量最多的是( )| A. | CH3Cl | B. | CHCl3 | C. | CCl4 | D. | HCl |
分析 甲烷与氯气的取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氯化氢,反应过程中,每取代甲烷中的1个H原子,都会同时生成1分子HCl气体,所以生成物中物质的量最大的是氯化氢.
解答 解:设甲烷和氯气的物质的量都是1mol,1mol甲烷和1mol氯气在光照条件下发生反应,生成有机物有CH3Cl、CH2Cl2、CHCl3、CCl4,根据碳原子守恒知,生成的各种氯代烃的物质的量都小于1mol,但生成的氯化氢的物质的量1mol,所以生成物的物质的量最多的产物是HCl,
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握甲烷取代反应的特点等为解答的关键,侧重分析与应用能力的考查,注意产物中含无机物HCl,题目难度不大.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
6.利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO.制备流程图如下:
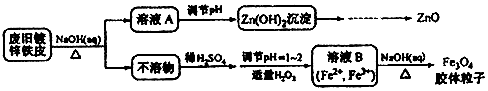
己知:Zn及其化合物的性质与Al及其化合物的性质相似.下列相关说法错误的是( )

己知:Zn及其化合物的性质与Al及其化合物的性质相似.下列相关说法错误的是( )
| A. | 用NaOH溶液处理废旧镀锌铁皮的作用是去除油污、溶解镀锌层 | |
| B. | 调节溶液A的pH产生Zn(OH)2沉淀,经抽滤、洗涤、灼烧即可制得ZnO | |
| C. | 由溶液B制得Fe3O4胶体粒子的过程中,须持续通N2,其原因是防止Fe2+被氧化 | |
| D. | Fe3O4胶体粒子能用减压过滤法实现固液分离 |
15.某化学反应2X(g)=Y(g)+Z(s)的能量变化如图所示.下列说法正确的是( )


| A. | 引发该反应一定需要加热或点燃等条件 | |
| B. | E1逆反应的活化能,E2是正反应的活化能 | |
| C. | 催化剂能减小E1和E2,但不改变反应的焓变 | |
| D. | X、Y、Z表示的反应速率之比为2:1:1 |
12.主链有5个碳原子,有四个甲基的烷烃有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
19.有机物分子中原子团间的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是( )
| A. | CH3COOH有酸性,而醇、酮类物质没有酸性 | |
| B. | 甲苯使酸性高锰酸钾褪色,而苯不能使其褪色 | |
| C. | 苯酚遇铁离子发生显色反应,而醇不能 | |
| D. | 乙醛与HCN发生加成反应,乙烯不能与之加成 |
9.设NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 1 mol乙烯和乙醇的混合物完全燃烧时消耗O2的分子数为3NA | |
| B. | 1.5 mol Na2O和Na2O2的混合物中离子数目为4.5 NA | |
| C. | 标准状况下,11.2 L HF中含有的分子数为0.5NA | |
| D. | 常温常压下,17 g 羟基含有的电子总数为9 NA |
13.化学在生产、生活中有着广泛的应用,下列物质的化学性质与应用的对应关系正确的是( )
| 化学性质 | 应用 | |
| A | O价铁具有还原性 | 铁粉可用于食品中的脱氧剂 |
| B | 明矾与NaOH生成Al(OH)3 | 明矾可作净水剂 |
| C | Fe的金属性比Cu活泼 | FeCl3浓溶液腐蚀Cu刻制印刷电路板 |
| D | NaHCO3水解显碱性 | 发酵粉中含有NaHCO3 |
| A. | A | B. | B | C. | C | D. | D |
7.科学家发现铂的两种化合物有不同的特性,a 具有抗癌作用,而 b 没有.则 a 和 b 属于( )


| A. | 同分异构体 | B. | 同素异形体 | C. | 同位素 | D. | 同系物 |
 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.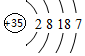 ,碘是紫黑色(填颜色)固体物质.(2)牙齿的损坏实际上是牙釉质羟基磷灰石[Ca5(PO4)3OH]溶解的结果,糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿.使用含氟牙膏会保护牙齿,因为氟离子会跟羟基磷灰石[Ca5(PO4)3OH]发生反应生成氟磷灰石,氟磷灰石比羟基磷灰石更能抵抗酸的侵蚀氟,用离子方程式表示这一过程Ca5(PO4)3OH(S)+F- (aq)?Ca5(PO4)3 F(S)+OH-(aq).此外氟离子还能抑制口腔细菌产生酸,含氟牙膏已经普遍使用.
,碘是紫黑色(填颜色)固体物质.(2)牙齿的损坏实际上是牙釉质羟基磷灰石[Ca5(PO4)3OH]溶解的结果,糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿.使用含氟牙膏会保护牙齿,因为氟离子会跟羟基磷灰石[Ca5(PO4)3OH]发生反应生成氟磷灰石,氟磷灰石比羟基磷灰石更能抵抗酸的侵蚀氟,用离子方程式表示这一过程Ca5(PO4)3OH(S)+F- (aq)?Ca5(PO4)3 F(S)+OH-(aq).此外氟离子还能抑制口腔细菌产生酸,含氟牙膏已经普遍使用.