��Ŀ����
20��J��L��M��R��T��ԭ��������������Ķ���������Ԫ�أ�J��R�����ڱ��е����λ�����ұ���JԪ��������ϼ۵ľ���ֵ����ԭ��������������ȣ�M�ǵؿ��к������Ľ���Ԫ�أ�| J | ||||
| R |
 ��Ԫ��T�����ڱ���λ�ڵڢ�A�壮
��Ԫ��T�����ڱ���λ�ڵڢ�A�壮��2��J������ɵĻ����������6��ԭ�ӣ���ṹ��ʽΪCH2=CH2��
��3��L�������̬�⻯���ˮ��Һ�Լ��ԣ�
�������ӹ�ҵ�У���ˮ��Һ������ʴ��H2O2 �����������������Ӧ�IJ��ﲻ��Ⱦ�������仯ѧ����ʽΪ2NH3��H2O+3H2O2�TN2��+8H2O��
��һ�������£����ڹ̶�������ܱ������з����ֽⷴӦ����H��0������ƽ����ı��±��з�Ӧ����x����ƽ����ϵ����x����y�ݼ�����bc��ѡ����ţ���
| ѡ�� | a | b | c | d |
| x | �¶� | �¶� | ����H2�����ʵ��� | ��������ʵ��� |
| y | ƽ�ⳣ��K | �����ʵ��� | ��ת���� | ���������ʵ����ܺ� |
��5���õ�ʽ��ʾR���⻯����NaOH��Һ��Ӧ���������ε���Һ����������Ũ��֮��Ĺ�ϵc��Na+��+c��H+��=c��OH-��+c��HS-��+2c��S2-����
���� JԪ��������ϼ۵ľ���ֵ����ԭ��������������ȣ�˵��J����ͻ��ϼ�������ϼ۾���ֵ��ȣ���J����������Ϊ4������J��R��Ϊ������Ԫ�ؿ�֪JΪCԪ�أ���RӦΪSԪ�أ�M�ǵؿ��к������Ľ���Ԫ�أ���MΪAlԪ�أ���T��ԭ����������S����Ϊ����������Ԫ�أ���TΪClԪ�أ�
��1��MΪAl�����Ӻ������Ϊ10��TΪCl��
��2��J������ɵĻ����������6��ԭ�ӣ�Ϊ��ϩ��
��3����һˮ�ϰ���������ⷴӦ���ɵ�����ˮ��
��a��Kֻ���¶��йأ�
b�������ֽ�Ϊ���ȷ�Ӧ�������¶�ƽ�������ƶ���
c������H2�����ʵ�����ƽ�������ƶ���
d�������ֽⷴӦΪ���ʵ�������ķ�Ӧ�����������ʵ�����ƽ��ʱ�����ʵ�������
��4���Ȼ���ˮ������HCl�ӷ������ˮ�����γɰ�����
��5��Na2S��Һ��������ˮ���Լ��ԣ�����Һ����ѭ����غ㣮
��� �⣺JԪ��������ϼ۵ľ���ֵ����ԭ��������������ȣ�˵��J����ͻ��ϼ�������ϼ۾���ֵ��ȣ���J����������Ϊ4������J��R��Ϊ������Ԫ�ؿ�֪JΪCԪ�أ���RӦΪSԪ�أ�M�ǵؿ��к������Ľ���Ԫ�أ���MΪAlԪ�أ���T��ԭ����������S����Ϊ����������Ԫ�أ���TΪClԪ�أ�
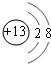
��1��M������ΪAl3+����ṹʾ��ͼΪ ��Ԫ��TΪClԪ�أ���Ԫ�������ڱ���λ�ڵڢ�A�壬
��Ԫ��TΪClԪ�أ���Ԫ�������ڱ���λ�ڵڢ�A�壬
�ʴ�Ϊ�� ����A��
����A��
��2��J������ɵĻ����������6��ԭ�ӣ�Ϊ��ϩ���ṹ��ʽΪCH2=CH2���ʴ�Ϊ��CH2=CH2��
��3����һˮ�ϰ���������ⷴӦ���ɵ�����ˮ����ӦΪ2NH3��H2O+3H2O2�TN2��+8H2O���ʴ�Ϊ��2NH3��H2O+3H2O2�TN2��+8H2O��
��a��Kֻ���¶��йأ���Ϊ���ȷ�Ӧ��x����y�ʲ�ѡ��
b�������ֽ�Ϊ���ȷ�Ӧ�������¶�ƽ�������ƶ�����x��y��С����ѡ��
c������H2�����ʵ�����ƽ�������ƶ�����x��y��С����ѡ��
d�������ֽⷴӦΪ���ʵ�������ķ�Ӧ�����������ʵ�����ƽ��ʱ�����ʵ���������x��y�ʲ�ѡ��
�ʴ�Ϊ��bc��
��4���Ȼ���ˮ������HCl�ӷ������ˮ�����γɰ�������ӦΪAlCl3+3H2O?Al��OH��3+3HCl�����ʴ�Ϊ��AlCl3+3H2O?Al��OH��3+3HCl����
��5��Na2S��Һ��������ˮ���Լ��ԣ���Һ��ѭ����غ㣬����������Ũ��֮��Ĺ�ϵΪc��Na+��+c ��H+��=c��OH-��+c��HS-��+2 c��S2-�����ʴ�Ϊ��c��Na+��+c ��H+��=c��OH-��+c��HS-��+2 c��S2-����
���� ���⿼��λ�á��ṹ�����ʣ�Ϊ��Ƶ���㣬����Ԫ�ص�λ�á����ʡ�Ԫ�ػ�����֪ʶΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�ⷴӦԭ����Ӧ�ã���3��Ϊ�����ѵ㣬��Ŀ�Ѷ��еȣ�

 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д�| A�� | ����ֱ���νṹ | |
| B�� | ����ԭ�Ӷ���ȡsp1�ӻ� | |
| C�� | NH3Ϊ�����νṹ��CO2Ϊֱ���νṹ | |
| D�� | ��ԭ�Ӻ�̼ԭ���϶�û�й¶Ե��� |
| A�� | 1s22s22P6 | B�� | 1s22s22P33s1 | C�� | 1s22s22P63s2 | D�� | 1s22s22P63s23P6 |
| A�� | �����Ǻ��� | B�� | ���Ǻ���ѿ�� | C�� | ���ۺ���ά�� | D�� | ��������춡�� |
| A�� | �÷�Ӧ���û���Ӧ | B�� | FeCl3�������� | ||
| C�� | Cu�ǻ�ԭ��������ʴ | D�� | �÷�Ӧ�������ӷ�Ӧ |
| A�� | �������ƿ�����DZͧ����������Դ | B�� | ����������������ص�ԭ�� | ||
| C�� | ��������������Ư�� | D�� | ��������Һ������ľ�ķ���� |
 ��ϸ�Ķ�ͼ����֪B��D��E��F��G�����������D���γ��������Ҫ��Ⱦ�F��K���⻯���F�ڳ�����ΪҺ̬��C��H���ճ���������Ϊ�����Ľ������ʣ�J����̬�ǽ������ʣ�O�ǰ�ɫ��������B��H��L��M��N��O�к���ͬ��Ԫ�أ�ͼ�в��ַ�Ӧ����������ȥ�����밴Ҫ��ش�
��ϸ�Ķ�ͼ����֪B��D��E��F��G�����������D���γ��������Ҫ��Ⱦ�F��K���⻯���F�ڳ�����ΪҺ̬��C��H���ճ���������Ϊ�����Ľ������ʣ�J����̬�ǽ������ʣ�O�ǰ�ɫ��������B��H��L��M��N��O�к���ͬ��Ԫ�أ�ͼ�в��ַ�Ӧ����������ȥ�����밴Ҫ��ش�