题目内容
9.下列有关物质用途的说法错误的是( )| A. | 过氧化钠可用作潜艇里氧气的来源 | B. | 二氧化硅是制造光电池的原料 | ||
| C. | 氯气可用于制造漂白粉 | D. | 硅酸钠溶液可用作木材防火剂 |
分析 A.过氧化钠与水或二氧化碳反应均生成氧气;
B.二氧化硅对光具有良好的全反射作用,Si为常见的半导体材料;
C.氯气与石灰乳反应制备漂白粉;
D.硅酸钠溶液不燃烧,不支持燃烧.
解答 解:A.过氧化钠与水或二氧化碳反应均生成氧气,则过氧化钠可用作潜艇里氧气的来源,故A正确;
B.二氧化硅对光具有良好的全反射作用,Si为常见的半导体材料,则硅是制造光电池的原料,故B错误;
C.氯气与石灰乳反应制备漂白粉,则氯气可用于制造漂白粉,故C正确;
D.硅酸钠溶液不燃烧,不支持燃烧,则硅酸钠溶液可用作木材防火剂,故D正确;
故选B.
点评 本题考查物质的组成、性质及应用,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意性质与用途的关系,题目难度不大.

练习册系列答案
 能力评价系列答案
能力评价系列答案
相关题目
20.J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
(1)M的离子结构示意图为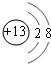 ;元素T在周期表中位于第ⅦA族.
;元素T在周期表中位于第ⅦA族.
(2)J和氢组成的化合物分子有6个原子,其结构简式为CH2=CH2.
(3)L的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3.H2O+3H2O2═N2↑+8H2O.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是bc(选填序号).
(4)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为:AlCl3+3H2O?Al(OH)3+3HCl↑.
(5)用等式表示R的氢化物与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-).
| J | ||||
| R |
 ;元素T在周期表中位于第ⅦA族.
;元素T在周期表中位于第ⅦA族.(2)J和氢组成的化合物分子有6个原子,其结构简式为CH2=CH2.
(3)L的最简单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为2NH3.H2O+3H2O2═N2↑+8H2O.
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是bc(选填序号).
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 平衡常数K | 甲的物质的量 | 甲的转化率 | 生成物物质的量总和 |
(5)用等式表示R的氢化物与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-).
17.已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,可与NaOH水溶液发生取代反应.1mol有机化合物与足量的NaOH溶液混合,在一定条件下反应,不考虑醇羟基与NaOH溶液的反应,则共消耗NaOH的物质的量( )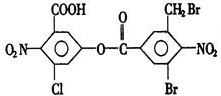

| A. | 5mol | B. | 6mol | C. | 7mol | D. | 8mol |
4.通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )
| A. | 硝酸钠 氢氧化钠 | B. | 氧化铜 二氧化锰 | ||
| C. | 氯化钾 二氧化锰 | D. | 硫酸铜 氢氧化钙 |
14.下列操作中不正确的是( )
| A. | 过滤时,玻璃棒与三层滤纸的一边接触 | |
| B. | 过滤时,漏斗下端紧贴烧杯内壁 | |
| C. | 分液时,上层液体要从分液漏斗上口倒出 | |
| D. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 |
18.下列说法不正确的是( )
| A. | 硝化甘油在体内能够分解出NO,少量的NO会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛 | |
| B. | TNT爆炸的方程式为:2C7H5N3O6(s)→6CO2(g)+5H2(g)+3N2(g)+8C(s),因而爆炸过程会产生大量的黑烟 | |
| C. | 为迎接G20峰会,全市努力植树造林,节能减排防治PM2.5,PM2.5是指大气中直径小于或等于2.5纳米的可吸入颗粒物 | |
| D. | 用中子轰击Hg核能发生下面的反应:80196Hg+01n→80197Hg→79197Au+e+制得金核,这个过程不属于化学变化 |