题目内容
11.氮化硅高温陶瓷材料是现代重要的结构陶瓷,因其有硬度大、熔点高、化学性质稳定等特点而受到广泛关注.工业上普遍用下列流程迸行生产: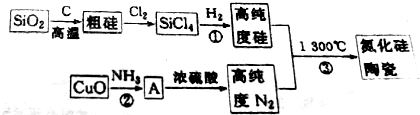
(1)SiO2和C反应除了得到粗硅外,还有可能得到一种硬度也很大的物质,是生成粗硅还是生成该物质主要是由C的用量决定的.
(2)反应①的条件是高温条件下隔绝空气.
(3)写出反应②的化学方程式3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
分析 (1)如果碳足量生成的硅与碳继续反应生成硬度也很大的物质碳化硅;
(2)氢气还原四氧化硅的反应条件是高温条件下隔绝空气;
(3)氨气还原氧化铜生成单质铜、氮气和水.
解答 解:(1)如果碳足量生成的硅与碳继续反应生成硬度也很大的物质碳化硅,所以与C的用量,故答案为:C的用量;
(2)氢气还原四氧化硅的反应条件是高温条件下隔绝空气,故答案为:高温条件下隔绝空气;
(3)氨气还原氧化铜生成单质铜、氮气和水,所以反应的化学方程式为:3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O,故答案为:3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
点评 本题考查硅和二氧化硅的性质,反应的化学方程式的书写和反应条件的考查,比较容易.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
1.下列离子方程式正确的是( )
| A. | 浓烧碱溶液中加入铝片:Al+4OH-=AlO2-+2H2O | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O | |
| C. | 用铁电极电解氯化铁溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| D. | 等体积、等浓度的Ba(OH)2稀溶解与NH4HCO3稀溶液混合Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O+H2O |
19.2.8g铁粉与高温水蒸气反应一段时间后,往固体剩余物中加入足量硝酸,得到NO和NO2混合气体0.672L(标准状况),则固体剩余物中未参加反应的铁有( )
| A. | 0.28g | B. | 1.4g | C. | 1.68g | D. | 2.1g |
6.下列各组物质之间的反应通常认为是可逆反应的是( )
| A. | 氢气在氧气中点燃 | |
| B. | 氮气与氢气在高温高压和有催化剂条件下反应 | |
| C. | 氢氧化钠溶液与盐酸混合 | |
| D. | 二氧化氮与氧气反应 |
3. 下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
 下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )
下列各组物质中,能一步实现如图所示①~⑤转化关系的是( )| X | Y | Z | W | |
| A | C | CO | CO2 | Na2CO3 |
| B | Fe3O4 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
 某草酸晶体的化学式可表示为H2C2O4•xH2O,为测定x的值,进行下列实验:
某草酸晶体的化学式可表示为H2C2O4•xH2O,为测定x的值,进行下列实验: