题目内容
19.2.8g铁粉与高温水蒸气反应一段时间后,往固体剩余物中加入足量硝酸,得到NO和NO2混合气体0.672L(标准状况),则固体剩余物中未参加反应的铁有( )| A. | 0.28g | B. | 1.4g | C. | 1.68g | D. | 2.1g |
分析 2.8g铁粉的物质的量为:$\frac{2.8g}{56g/mol}$=0.05mol,0.672L(标准状况)的物质的量为:$\frac{0.672L}{22.4L/mol}$=0.03mol,如果0.03mol全部是二氧化氮固体剩余物转移电子数为0.03mol,若0.03mol全部是一氧化氮固体剩余物转移电子数为0.09mol,根据得失电子守恒,分析解答.
解答 解:2.8g铁粉的物质的量为:$\frac{2.8g}{56g/mol}$=0.05mol,0.672L(标准状况)的物质的量为:$\frac{0.672L}{22.4L/mol}$=0.03mol,如果0.03mol全部是二氧化氮固体剩余物转移电子数为0.03mol,若0.03mol全部是一氧化氮固体剩余物转移电子数为0.09mol,设生成的四氧化三铁的物质的量为xmol,则固体剩余物中未参加反应的铁的物质的量为(0.05-3x)mol,所以与硝酸反应提供电子的物质的量为:[(0.05-3x)×3+x]mol,根据得失电子守恒得0.03<(0.05-3x)×3+x<0.09,所以0.0075<x<0.015,则0.005<0.05-3x<0.0275,铁的质量取值范围为:0.005×56<m<0.0275×56,也就是0.28g<m<1.54g,故选B.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应及电子守恒、原子守恒的计算为解答的关键,侧重分析能力与计算能力的综合考查,题目难度中等.

练习册系列答案
相关题目
10.向下列溶液中逐渐通入SO2,一直不产生沉淀的是( )
| A. | Ca(OH)2溶液 | B. | CaCl2溶液 | C. | Ba(NO3)2溶液 | D. | H2S的水溶液 |
7. 角鲨烯是一种脂质不皂化物,最初从角鲨烯的甘油中发现的,具有生物氧化还原作用与提高能量的效果,有利于增强机体的耐力与改善心脏功能,可用于癌症的防治,是一种无毒性的具有防病治病作用的海洋生物活性物质,关于角鲨烯有下列叙述:
角鲨烯是一种脂质不皂化物,最初从角鲨烯的甘油中发现的,具有生物氧化还原作用与提高能量的效果,有利于增强机体的耐力与改善心脏功能,可用于癌症的防治,是一种无毒性的具有防病治病作用的海洋生物活性物质,关于角鲨烯有下列叙述:
①能使酸性高锰酸钾溶液褪色
②能与氢气发生加成反应
③角鲨烯只含碳、氢两种元素
④角鲨烯能发生取代反应.
其中正确的是( )
 角鲨烯是一种脂质不皂化物,最初从角鲨烯的甘油中发现的,具有生物氧化还原作用与提高能量的效果,有利于增强机体的耐力与改善心脏功能,可用于癌症的防治,是一种无毒性的具有防病治病作用的海洋生物活性物质,关于角鲨烯有下列叙述:
角鲨烯是一种脂质不皂化物,最初从角鲨烯的甘油中发现的,具有生物氧化还原作用与提高能量的效果,有利于增强机体的耐力与改善心脏功能,可用于癌症的防治,是一种无毒性的具有防病治病作用的海洋生物活性物质,关于角鲨烯有下列叙述:①能使酸性高锰酸钾溶液褪色
②能与氢气发生加成反应
③角鲨烯只含碳、氢两种元素
④角鲨烯能发生取代反应.
其中正确的是( )
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
14.欲将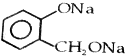 转化为
转化为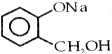 ,可以加入( )
,可以加入( )
 转化为
转化为 ,可以加入( )
,可以加入( )| A. | 水 | B. | 碳酸氢钠溶液 | C. | 碳酸 | D. | 盐酸 |
16.氰气分子式为(CN)2,其性质与卤素相似,在化学上称为类卤化合物,以下关于(CN)2的叙述错误的是( )
| A. | 可与活泼金属直接发生化学反应 | B. | 可溶于水,易溶于NaOH溶液 | ||
| C. | 是一种无毒气体 | D. | 可用HCN溶液与MnO2混合加热制取 |
 化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含 淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.(已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O)
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求.某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KBr、KI(含 淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好.(已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O)