题目内容
2.下列叙述错误的是( )| A. | 任何条件下,等物质的量O2的和CO所含的分子数必相等 | |
| B. | 0.012 kg 12C 含有约6.02×1023个碳原子 | |
| C. | 在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类 | |
| D. | CH4的摩尔质量为16g |
分析 A.分子数与温度和压强无关,分子数=nNA;
B.将12g12C中含有的碳原子个数称为阿伏伽德罗常数;
C.物质的量是表示微观粒子的物理量,需要表明微粒种类;
D.摩尔质量单位是g/mol.
解答 解:A.分子数与温度和压强无关,根据N=nNA知,分子数与物质的量成正比,所以任何条件下,等物质的量O2的和CO所含的分子数必相等,故A正确;
B.将12g12C中含有的碳原子个数称为阿伏伽德罗常数,即0.012kg碳-12含有约6.02×1023个碳原子,故B正确;
C.物质的量是表示微观粒子的物理量,需要表明微粒种类,所以在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类,故C正确;
D.摩尔质量的单位是g/mol,甲烷的摩尔质量是16g/mol,故D错误;
故选D.
点评 本题考查物质的量的有关知识,明确阿伏伽德罗常数含义、摩尔质量单位等知识点是解本题关键,熟练掌握物质的量有关公式,注意:只有计算气体体积时才与温度压强有关,计算分子数、质量、物质的量浓度等时与温度压强无关.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
12.从KNO3和少量NaCl杂质的混合物中提纯KNO3.涉及的操作依次有:①溶解、②过滤、③结晶、④冷却、⑤蒸发浓缩.其中合理的是( )
| A. | ①②③④⑤ | B. | ①③⑤④② | C. | ①⑤④③② | D. | ①②⑤③④ |
13.在某温度下,可逆反应mA(g)+nB(g)?pC(g)+qD(g)的平衡常数为K,下列说法正确的是( )
| A. | K越大,反应达到平衡时所用的时间越短 | |
| B. | K越小,达到平衡时,反应物的 转化率越大 | |
| C. | K随反应物浓度改变而改变 | |
| D. | K越大,达到平衡时,反应进行的程度越大 |
10.下列实验方法不正确的是( )
| A. | 用澄清石灰水鉴别Na2CO3和NaHCO3溶液 | |
| B. | 用焰色反应鉴别NaCl和KCl | |
| C. | 用丁达尔效应鉴别硫酸钠溶液和硅酸胶体 | |
| D. | 用排水集气法收集NO |
17.将112mL乙炔溶于2mol苯中,再加入30g苯乙烯,所得混合物的含碳的质量分数为( )
| A. | 92.3% | B. | 75% | C. | 66.75% | D. | 不能确定 |
7.下列变化需要加入还原剂才能实现的( )
| A. | MnO2→Mn2+ | B. | CO→CO2 | C. | Cu→Cu2+ | D. | Cl2→Cl- |
14.化学与生产、生活、科技、环境等密切相关,下列说法不正确的是( )
| A. | 用蘸有浓氨水的棉棒检验输送氯气的管道是否漏气 | |
| B. | 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 | |
| C. | 大力实施矿物燃料脱硫脱硝技术,能减少二氧化硫、氮氧化物的排放 | |
| D. | 纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附. |
14.乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味.实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:

实验步骤:
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热A,回流50min.反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是球形冷凝管.
(2)在洗涤操作中,第一次水洗的主要目的是洗掉大部分硫酸和醋酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是提高醇的转化率.
(5)实验中加入少量无水MgSO4的目的是干燥.
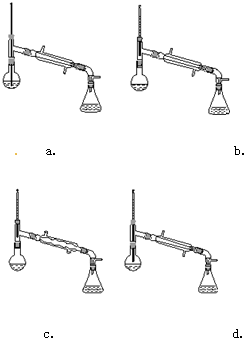
(6)在蒸馏操作中,仪器选择及安装都正确的是b(填标号).
(7)本实验的产率是c(填标号).
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”),其原因是会收集少量未反应的异戊醇.

| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戍醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热A,回流50min.反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g.
回答下列问题:
(1)仪器B的名称是球形冷凝管.
(2)在洗涤操作中,第一次水洗的主要目的是洗掉大部分硫酸和醋酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后d(填标号).
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是提高醇的转化率.
(5)实验中加入少量无水MgSO4的目的是干燥.
(6)在蒸馏操作中,仪器选择及安装都正确的是b(填标号).
(7)本实验的产率是c(填标号).
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏高(填“高”或“低”),其原因是会收集少量未反应的异戊醇.