题目内容
20.工业上可以以煤和水为原料通过一系列转化变为清洁能源氢气或工业原料甲醇.(1)用煤制取氢气的反应是:C(s)+2H2O(g)$\frac{\underline{\;高温\;}}{\;}$ CO2(g)+2H2(g)△H>0
若已知碳的燃烧热a和氢气的燃烧热b不能(填“能”或“不能”)求出上述反应的△H.若能则求出其△H(若不能请说明理由):因为上述反应与氢气燃烧热的反应中水的状态不同.
(2)工业上也可以仅利用上述反应得到的CO2和H2进一步合成甲醇,反应方程式为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,
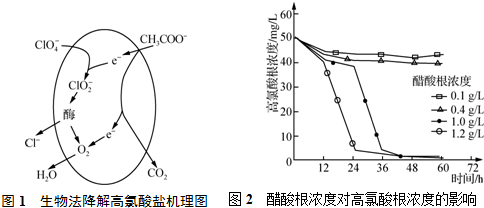
在一恒温恒容密闭容器中充入1mol CO2和3 mol H2进行上述反应.测得CO2和CH3OH(g)浓度随时间变化如图1所示.
ⅰ.该温度下的平衡常数为5.33.10min后,保持温度不变,向该密闭容器中再充入1mol CO2(g)和1mol H2O(g),则平衡正向(填“正向”、“逆向”或“不”)移动.
ⅱ.对于基元反应aA+bB?cC+dD而言,其某一时刻的瞬时速率计算公式如下:正反应速率为V正=k正•c(A)a•c(B)b;逆反应速率为V逆=k逆•c(C)c•c(D)d其中k正、k逆为速率常数.求该反应进行到第10min时k逆:k正=3:16.
(3)工业上利用水煤气合成甲醇燃料,反应为CO(g)+2H2(g)?CH3OH(g)△H<0.在一定条件下,将l mol CO和2mol H2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图2所示:
①平衡时,M点CH3OH的体积分数为10%.则CO的转化率为25%.
②X轴上a点的数值比b点小(填“大”或“小”).Y轴表示温度(填“温度”或“压强”),判断的理由是随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,平衡逆向移动,故Y表示温度.

分析 (1)反应热与物质的聚集状态有关,聚集状态不同,反应热不同;
(2)ⅰ.计算平衡时氢气、水的浓度,再根据K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$计算平衡常数;
保持温度不变,向该密闭容器中再充入1mol CO2(g)和1mol H2O(g),相当于增大压强,增压平衡向气体系数小的方向移动;
ⅱ.平衡时满足V正=V逆,v正=k正•c(A)a•c(B)b;V逆=k逆•c(C)c•c(D)d,则k逆:k正=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$=K;
(3)①根据三行式计算得到;
②根据图示信息:X轴上a点的数值比b点小,随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,结合平衡移动原理回答.
解答 解:(1)反应热与物质的聚集状态有关,聚集状态不同,反应热不同,上述反应与氢气燃烧热的反应中水的状态不同,所以不能求出上述反应的焓变;
故答案为:不能;因为上述反应与氢气燃烧热的反应中水的状态不同;
(2)ⅰ平衡时甲醇为0.75mol/L、二氧化碳为0.25mol/L,则:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始浓度(mol/L):1 3 0 0
变化浓度(mol/L):0.75 2.25 0.75 0.75
平衡浓度(mol/L):0.50 0.75 0.75 0.75
则平衡常数K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$=$\frac{0.75×0.75}{0.25×0.7{5}^{2}}$=$\frac{16}{3}$=5.33;
保持温度不变,向该密闭容器中再充入1mol CO2(g)和1mol H2O(g),相当于增大压强,增压平衡向气体系数小的方向移动,即向正方向移动;
故答案为:5.33;正向;
ⅱ平衡时满足V正=V逆,v正=k正•c(A)a•c(B)b;V逆=k逆•c(C)c•c(D)d,
则k逆:k正=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$=K=3:16;
故答案为:3:16;
(3)①设CO的转化量是x,则
CO(g)+2H2(g)?CH3OH(g);
初始量:1mol 2mol 0
变化量:x 2x x
平衡量:1-x 2-2x x
平衡时,CH3OH的体积分数为10%,则$\frac{x}{1-x+2-2x+x}$×100%=10%,x=0.25,所以CO的转化率为$\frac{0.25mol}{1mol}$×100%=25%,故答案为:25%;
②根据图示信息:X轴上a点的数值比b点小,随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,平衡逆向移动,故Y表示温度,故答案为:小;温度;随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,平衡逆向移动,故Y表示温度.
点评 本题为综合题,涉及反应热的计算、化学平衡平衡移动影响因素、化学平衡常数计算、平衡移动原理的应用,题目难度中等,明确化学平衡常数的概念及表达式为解答关键,本题也可以利用三段式计算,试题培养了学生的分析能力及化学计算能力.

| A. | 水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物 | |
| B. | 下雪后,常用播撒NaCl颗粒方法来防止道路结冰 | |
| C. | 用活性炭为糖浆脱色和用SO2漂白纸浆的原理不同 | |
| D. | 在医学上用BaSO4做钡餐,是因为Ba2+对人体无毒 |
| 反应 | △H(kJ•mol-1) | 平衡常数(K) |
| 4NH3 (g)+5O2 (g)?4NO (g)+6H2O (g) | -905.5 | 1.1×1026mol•L-1 |
| 4NH3 (g)+4O2 (g)?2N2O (g)+6H2O (g) | -1104.9 | 4.4×1028 |
| 4NH3 (g)+3O2 (g)?2N2 (g)+6H2O (g) | -1269.0 | 7.1×1034L•mol-1 |
(2)图1表示在密闭体系中进行实验,测定不同温度下,在相同时间内各组分的浓度.

①图中a、b、c三点,主反应速率最大的是c.
②试解释N2浓度曲线先上升后下降的原因先上升:反应还未到达平衡状态,温度越高,化学反应速率越快,单位时间内N2浓 度越大;后下降:达到平衡状态后,随着温度升高,因反应正向放热,平衡逆向移动,且随温度升高有副产物的生成,N2浓度降低.
③550K时,欲提高N2O的百分含量,应采取的措施是采用合适的催化剂.
(3)为探究碳基催化剂中Fe、Mn、Ni等元素的回收,将该催化剂溶解后得到含有Fe2+、Mn2+、Ni2+的溶液,物质的量浓度均为10-3mol•L-1.欲完全沉淀Fe2+、Mn2+(离子浓度低于1.0×10-6),应控制CO32-的物质的量浓度范围为(3.0×10-5,1.0×10-4 ).
| 沉淀物 | Ksp |
| FeCO3 | 3.0×10-11 |
| MnCO3 | 2.0×10-11 |
| NiCO3 | 1.0×10-7 |
a为外接电源的负极(填“正”、“负”).通入NO的电极反应式为2NO+4e-=N2+2O2-.
| A. | 向纯水中投入一小块金属钠 | B. | 将水加热煮沸 | ||
| C. | 向水中通入SO2 | D. | 向水中加入NaCl |
| A. | 氢气、天然气 | B. | 液化气、核能 | C. | 太阳能、风能 | D. | 燃煤、97#汽油 |
| A. | 1 mol H2O中所含的粒子数目一定是NA | |
| B. | 1 molNH4+所含的质子数是10NA | |
| C. | 51 g NH3所含原子数为3NA | |
| D. | 氧气的相对分子质量与2NA个氧原子质量(以g为单位)在数值上相等 |

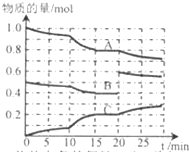 在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:
在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题: