题目内容
下列物质属于含有共价键的离子化合物的是( )
| A、NH4Cl |
| B、Na2O |
| C、Al2O3 |
| D、SO3 |
考点:离子化合物的结构特征与性质
专题:
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,铵根离子和酸根离子之间存在离子键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,据此分析解答.
解答:
解:A.氯化铵中铵根离子和氯离子之间存在离子键,铵根离子中N原子和H原子之间存在共价键,故A正确;
B.氧化钠中钠离子和氧离子之间存在离子键,为离子化合物,故B错误;
C.氧化铝中铝离子和氧离子之间存在离子键,为离子化合物,故C错误;
D.三氧化硫中O原子和S原子之间只存在共价键,为共价化合物,故D错误;
故选A.
B.氧化钠中钠离子和氧离子之间存在离子键,为离子化合物,故B错误;
C.氧化铝中铝离子和氧离子之间存在离子键,为离子化合物,故C错误;
D.三氧化硫中O原子和S原子之间只存在共价键,为共价化合物,故D错误;
故选A.
点评:本题考查化学键的判断,侧重考查基本概念,明确离子键和共价键的区别是解本题关键,注意配位键属于共价键,题目难度不大.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
下列说法正确的是( )
| A、糖类、油脂和蛋白质是基本营养物质 |
| B、蛋白质水解的最终产物是多肽 |
| C、糖尿病人不能食用含糖和淀粉的食品 |
| D、向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
已知25℃、101kPa下,拆开1mol C-H键要吸收415kJ的能量,拆开1mol C-C键要吸收331kJ的能量,拆开1mol O2中的O═O键要吸收498kJ的能量,形成水分子中的1mol H-O键要放出465kJ的能量,形成二氧化碳分子中的1mol C═O键要放出798kJ的能量.在丙烷燃烧过程中不考虑其他能量转化,下列说法正确的是( )
| A、丙烷完全燃烧的热化学方程式为C3H8+5O2═3CO2+4H2O△H=-2 036 kJ/mol |
| B、C3H8(g)+5O2(g)═3CO2(g)+4H2O(g);△H<-2 036 kJ/mol |
| C、丙烷完全燃烧的热化学方程式为:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=2 036 kJ/mol |
D、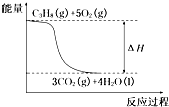 丙烷燃烧的能量变化可用如图所示表示 |
关于3Cl2+6KOH
KClO3+5KCl+3H2O反应,以下说法错误的是( )
| ||
| A、Cl2既是氧化剂,又是还原剂 |
| B、3 mol氯气参加反应转移5 mol电子 |
| C、氧化产物的物质的量是还原产物的物质的量的5倍 |
| D、每有1 mol原子被氧化的同时就有5 mol原子被还原 |
下列有关物质性质说法不正确的是( )
| A、热稳定性:HCl>HI |
| B、原子半径:Na>K |
| C、元素的最高正价:S>Si |
| D、氧化性:Br2<Cl2 |
你认为下列数据可信的是(已知1nm=10-9m)( )
| A、某元素的原子半径是0.160 nm |
| B、某常见气体的密度为1.8 g/cm3 |
| C、某澄清石灰水的浓度是4.0 mol/L |
| D、某溶液中溶质的质量分数120% |
如图是模拟工业电解饱和食盐水的装置图,下列叙述不正确的是( )


| A、a 为电源的负极 | ||||
| B、Fe电极的电极反应是4OH--4e-=2H2O+O2↑ | ||||
| C、通电一段时间后,铁电极附近溶液先变红 | ||||
D、电解饱和食盐水的化学方程式是2NaCl+2H2O
|
 实验室需要0.5mol?L-1硫酸溶液480ml.根据这两种溶液的配制情况回答下列问题:
实验室需要0.5mol?L-1硫酸溶液480ml.根据这两种溶液的配制情况回答下列问题: