题目内容
20.下列离子方程式中,正确的是( )| A. | 稀硫酸与NaOH溶液反应:2H++OH-=H2O | |
| B. | AgNO3溶液与NaCl溶液反应:Ag++Cl-=AgCl↓ | |
| C. | CaCO3与稀盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | Fe片插入FeCl3溶液中:Fe+Fe3+=2Fe2+ |
分析 A.反应生成硫酸钠和水,电荷不守恒;
B.反应生成氯化银和硝酸钠;
C.碳酸钙在离子反应中保留化学式;
D.电子、电荷不守恒.
解答 解:A.稀硫酸与NaOH溶液反应的离子反应为H++OH-=H2O,故A错误;
B.AgNO3溶液与NaCl溶液反应的离子反应为Ag++Cl-=AgCl↓,故B正确;
C.CaCO3与稀盐酸反应的离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,故C错误;
D.Fe片插入FeCl3溶液中的离子反应为Fe+2Fe3+=3Fe2+,故D错误;
故选B.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
11.以下对核外电子运动状况描述正确的是( )
| A. | 能量低的电子只能在s轨道上运动,能量高的电子总在f轨道上运动 | |
| B. | 电子的运动和行星相似,围绕着原子核在固定的轨道上高速旋转 | |
| C. | 同一能层中不同能级的能量高低相同 | |
| D. | M能层中含有3d能级 |
8.某烃苯环上的一氯代物只有2种,则该烃是( )
| A. |  | B. |  | C. |  | D. |  |
15.W、X、Y、Z均为短周期元素,原子序数依次增加,W的原子核最外层电子数是次外层的2倍,X-、Y+具有相同的电子层结构,Z的阴离子不能发生水解反应.下列说法正确的是( )
| A. | 原子半径:Y>Z>X>W | |
| B. | 简单氢化物的稳定性:X>Z>W | |
| C. | 最高价氧化物的水化物的酸性:W>Z | |
| D. | X可分别与W、Y形成化合物,其所含的化学键类型相同 |
12.下列反应中,在原理上可以设计成原电池的是( )
| A. | Ba(OH)2•8H2O与NH4Cl的反应 | B. | 铝片与浓硫酸的反应 | ||
| C. | 甲烷与氧气的反应 | D. | 石灰石的分解反应 |
10.我们能在昏暗的光线下看见物体,离不开视网膜中一种叫“视黄醛”(见甲)的有机化合物,而与视黄醛相似结构的维生素A(见乙)常作为保健药物.则下列有关叙述正确的是( )


| A. | 视黄醛的分子式为C21H26O | |
| B. | 维生素A分子结构中含有苯环、碳碳双键和羟基 | |
| C. | 维生素A是视黄醛的氧化产物 | |
| D. | 1 mol视黄醛在一定条件下最多能与6 mol H2发生反应 |
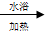 CH3CH2COONH4+3NH3+2Ag+H2O.在此过程中丙醛发生氧化(氧化、还原)反应,此反应可以检验醛基的存在.
CH3CH2COONH4+3NH3+2Ag+H2O.在此过程中丙醛发生氧化(氧化、还原)反应,此反应可以检验醛基的存在.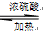 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.