题目内容
15.W、X、Y、Z均为短周期元素,原子序数依次增加,W的原子核最外层电子数是次外层的2倍,X-、Y+具有相同的电子层结构,Z的阴离子不能发生水解反应.下列说法正确的是( )| A. | 原子半径:Y>Z>X>W | |
| B. | 简单氢化物的稳定性:X>Z>W | |
| C. | 最高价氧化物的水化物的酸性:W>Z | |
| D. | X可分别与W、Y形成化合物,其所含的化学键类型相同 |
分析 W、X、Y、Z均为短周期元素,原子序数依次增加,W的原子核最外层电子数是次外层的2倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为4,故W为C元素;X-、Y+具有相同的电子层结构,二者原子序数均大于碳,结合离子电荷可知X为F元素、Y为Na;Z的阴离子不能发生水解反应,则Z为Cl.
解答 解:W、X、Y、Z均为短周期元素,原子序数依次增加,W的原子核最外层电子数是次外层的2倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为4,故W为C元素;X-、Y+具有相同的电子层结构,二者原子序数均大于碳,结合离子电荷可知X为F元素、Y为Na;Z的阴离子不能发生水解反应,则Z为Cl.
A.同周期自左而右原子半径减小,一般电子层越多原子半径越大,故原子半径:Y(Na)>Z(Cl)>W(C)>X(F),故A错误;
B.非金属性F>Cl>C,非金属性越强,氢化物越稳定性,故氢化物稳定性:HF>HCl>CH4,故B正确;
C.非金属性Cl>C,非金属性越强,最高价含氧酸的酸性越强,故酸性:HClO4>CH2CO3,故C错误;
D.CF4为共价化合物,而NaF为离子化合物,故D错误.
故选:B.
点评 本题考查结构性质位置关系应用,侧重对元素周期律的考查,推断元素是解题关键,注意对基础知识的理解掌握.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
10.下列说法中不正确的是( )
| A. | 临氯甲苯、1,2-二氯乙烷、3-甲基-1-丁烯的结构简式分别为: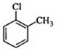 CH2Cl-CH2Cl CH2Cl-CH2Cl 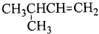 | |
| B. | 2,3,4一三甲基戊烷的核磁共振氢谱中出现五组峰 | |
| C. | 3,4一二甲基己烷的一氯代产物有4种 | |
| D. | 甲苯、硝基苯、2-甲基丙烯分子中的所有碳原子处于同一平面上 |
20.下列离子方程式中,正确的是( )
| A. | 稀硫酸与NaOH溶液反应:2H++OH-=H2O | |
| B. | AgNO3溶液与NaCl溶液反应:Ag++Cl-=AgCl↓ | |
| C. | CaCO3与稀盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | Fe片插入FeCl3溶液中:Fe+Fe3+=2Fe2+ |
7. Ⅰ.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见下表:用10mLH2O2制取150mLO2所需的时间(秒)
Ⅰ.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见下表:用10mLH2O2制取150mLO2所需的时间(秒)
(1)该小组在设计方案时,考虑了浓度、催化剂、温度等因素对过氧化氢分解速率的影响.
(2)从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?一般加入催化剂、反应速率加快(或升高温度反应速率加快,降低温度反应速率减慢;增加反应物浓度,反应速率加快,减小反应物浓度,反应速率减慢).
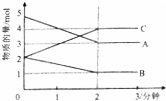
Ⅱ.反应在体积为5L的恒容密闭容器中进行,在0-3分钟内个物质的量的变化情况如图所示,(A,B,C均为气体,且A气体有颜色).
(3)该反应的化学方程式为2A+B?2C.
(4)反应开始至2分钟时,B的平均速率为0.1mol/(L•min).
(5)能说明该反应已达到平衡状态的是cd.
a.v(A)=2v(B) b.容器内各物质的物质的量相等 c.v逆(A)=v正(C) d.容器内气体的颜色保持不变.
 Ⅰ.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见下表:用10mLH2O2制取150mLO2所需的时间(秒)
Ⅰ.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见下表:用10mLH2O2制取150mLO2所需的时间(秒) 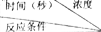 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 260 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
(2)从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?一般加入催化剂、反应速率加快(或升高温度反应速率加快,降低温度反应速率减慢;增加反应物浓度,反应速率加快,减小反应物浓度,反应速率减慢).
Ⅱ.反应在体积为5L的恒容密闭容器中进行,在0-3分钟内个物质的量的变化情况如图所示,(A,B,C均为气体,且A气体有颜色).
(3)该反应的化学方程式为2A+B?2C.
(4)反应开始至2分钟时,B的平均速率为0.1mol/(L•min).
(5)能说明该反应已达到平衡状态的是cd.
a.v(A)=2v(B) b.容器内各物质的物质的量相等 c.v逆(A)=v正(C) d.容器内气体的颜色保持不变.
4.氧杂环丙烷的结构如图所示,下列说法正确的是( )
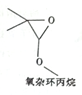

| A. | 该有机物能与金属钠反应 | |
| B. | 该有机物的分子式为C5H9O2 | |
| C. | 该有机物的同分异构体(不考虑立体异构)中,属于羧酸的物质共有5种 | |
| D. | 该有机物的同分异构体(不考虑立体异构体)中,能水解生成羧酸与醇的物质共有9种 |
5.现有部分短周期元素的性质或原子结构如表:
(1)元素X位于元素周期表的第二周期第IVA族,
(2)元素Y的原子结构示意图为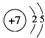 ,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量试样加入到试管中,加入氢氧化钠溶液,加热,在试管口用湿润的红色石蕊试纸检验放出气体,试纸由红变蓝.
,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量试样加入到试管中,加入氢氧化钠溶液,加热,在试管口用湿润的红色石蕊试纸检验放出气体,试纸由红变蓝.
(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应.
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层上电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y的原子结构示意图为
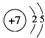 ,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量试样加入到试管中,加入氢氧化钠溶液,加热,在试管口用湿润的红色石蕊试纸检验放出气体,试纸由红变蓝.
,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量试样加入到试管中,加入氢氧化钠溶液,加热,在试管口用湿润的红色石蕊试纸检验放出气体,试纸由红变蓝.(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应.