题目内容
15.将浑浊的河水制成蒸馏水,正确的方法是( )| A. | 过滤 | B. | 蒸发 | ||
| C. | 先过滤后蒸馏 | D. | 加入某种药品溶解浑浊的固体 |
分析 用自来水制成蒸馏水应用蒸馏的方法分离,如溶液浑浊,应先过滤.
解答 解:如是悬浊液,则可直接蒸馏,如是乳浊液,应先过滤后再蒸馏,且防止在加热时悬浮物分解或挥发导致蒸馏水不纯,故选C.
点评 本题考查物质的分离、提纯,为高频考点,把握水的沸点及混合物分离方法为解答的关键,易错点为D,注意悬浮物的性质的可能性,题目难度不大.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
5.除去下列物质中所含的杂质(括号内为杂质),将选用的试剂和有关离子方程式填在题后的横线上.
| 混合物成分 | 提纯试剂 | 离子方程式 |
| ①FeCl2溶液(FeCl3) | ||
| ②FeCl3溶液(FeCl2) | ||
| ③Na2CO3溶液(NaHCO3) | ||
| ④Fe2O3(Al2O3) |
6.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1L2mol•L-1的(NH4)2S溶液中含有的S2-数目为0.2NA | |
| B. | 7.8g苯中含有C=C键数目为0.3NA | |
| C. | 常温常压下,5.6g乙烯和环丙烷的混合气体中含有的碳原子数为0.4NA | |
| D. | 用惰性电极电解1L浓度均为2mol•L-1的AgNO3与Cu(NO3)2的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4g金属 |
3.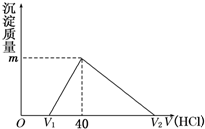 将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如下图所示,则下列选项正确的是( )
将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如下图所示,则下列选项正确的是( )
 将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如下图所示,则下列选项正确的是( )
将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如下图所示,则下列选项正确的是( )| A. | 图中m值为1.56 g | B. | 标准状况下产生氢气896 mL | ||
| C. | 图中V2为60 mL | D. | 原合金质量为0.92 g |
10.已知反应:PC15(g)?PC13(g)+C12(g),将1.0mol PC15充入容积为2L的密闭容器中,一段时间后,测得PC15的浓度为0.3mol/L,在这段时间内的平均反应速率υ(PC15)=0.4mol/(L•min),则这段时间为( )
| A. | 50 s | B. | 30 s | C. | 5 s | D. | 1 s |
7.将适量金属钠投入下列物质的溶液中,有气体放出,但一定无沉淀生成的是( )
| A. | HCl | B. | 饱和NaOH溶液 | C. | FeCl3 | D. | AlCl3 |