题目内容
下列反应的离子方程式正确的是( )
| A、钠与水反应:Na+H2O═Na++OH-+H2↑ |
| B、硫化钠水解:S2-+2H2O?H2S+2OH- |
| C、稀硫酸与氢氧化钡溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
| D、碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A、根据质量守恒定律判断,离子方程式两边氢原子个数不相等;
B、硫离子水解分步进行,主要以第一步为主;
C、稀硫酸与氢氧化钡反应生成硫酸钡沉淀和弱电解质水;
D、醋酸为弱电解质,离子方程式中应该保留分子式.
B、硫离子水解分步进行,主要以第一步为主;
C、稀硫酸与氢氧化钡反应生成硫酸钡沉淀和弱电解质水;
D、醋酸为弱电解质,离子方程式中应该保留分子式.
解答:
解:A、钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B、硫化钠水解的离子方程式,只写第一步,其正确离子方程式为:S2-+H2O?HS-+OH-,故B错误;
C、稀硫酸与氢氧化钡溶液反应生成硫酸钡和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C正确;
D、碳酸钙与醋酸反应,醋酸应该保留分子式,正确的离子方程为:CaCO3+2CH3COOH═2CH3COO-+Ca2++H2O+CO2↑,故D错误;
故选C.
B、硫化钠水解的离子方程式,只写第一步,其正确离子方程式为:S2-+H2O?HS-+OH-,故B错误;
C、稀硫酸与氢氧化钡溶液反应生成硫酸钡和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C正确;
D、碳酸钙与醋酸反应,醋酸应该保留分子式,正确的离子方程为:CaCO3+2CH3COOH═2CH3COO-+Ca2++H2O+CO2↑,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,属于中等难度的试题,侧重对学生能力的培养和训练;注意明确判断离子方程式正误常用方法:(1)检查反应能否发生;(2)检查反应物、生成物是否正确;(3)检查各物质拆分是否正确;(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等);(5)检查是否符合原化学方程式.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目

 ,关于它的下列说法正确的是
,关于它的下列说法正确的是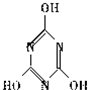 ).三聚氰酸可看成是三分子氰酸通过加成反应得到的环状分子,则氰酸的结构式是
).三聚氰酸可看成是三分子氰酸通过加成反应得到的环状分子,则氰酸的结构式是 A~F是中学常见物质,其中B、D、F均为单质,它们的相互转化关系如图所示:
A~F是中学常见物质,其中B、D、F均为单质,它们的相互转化关系如图所示:

