题目内容
2.标准状态下,现在一固定容积的容器盛满NO、O2、NO2混合气体,将该容器倒置在水中,充分反应后无剩余气体,所得溶液的物质的量为m mol/L则m( )| A. | $\frac{1}{39.2}$<m<$\frac{1}{28}$ | B. | $\frac{1}{39.2}$<m<33.6 | C. | 0<m<$\frac{1}{22.4}$ | D. | $\frac{1}{28}$<$\frac{1}{22.4}$ |
分析 将NO、NO2、O2三种气体按一定比例充满一固定容积的容器,并将该容器倒置在水槽中,充分反应后,容器中无气体剩余,可能发生:4NO2+O2+2H2O=4HNO3或4NO+3O2+2H2O=4HNO3,所得溶液为HNO3溶液,利用端值法解答.
解答 解:若混合气体是NO2和O2,且体积比为4:1,因为发生反应:4NO2+O2+2H2O=4HNO3,生成硝酸的物质的量是溶于水的气体物质的量的$\frac{4}{5}$,所得溶液的体积等于溶于水的气体体积,所以所得溶液的物质的量浓度为$\frac{4}{5×22.4}$mol/L=$\frac{1}{28}$mol/L;
若混合气体是NO和O2,且二者体积比为3:4,因为发生反应:4NO+3O2+2H2O=4HNO3,生成硝酸的物质的量是溶于水的气体物质的量的$\frac{4}{7}$,所得溶液体积等于溶于水的气体体积,所得溶液的物质的量浓度为$\frac{4}{7×22.4}$moL/L=$\frac{1}{39.2}$mol/L,
因是三种物质的混合物,应介于二者之间,
故选A.
点评 本题是有关NO2、NO和O2混合气体溶于水的计算问题,要解决这类问题应注意利用端值法结合反应的化学方程式计算,题目难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1).

关于两容器中反应的说法正确的是( )

关于两容器中反应的说法正确的是( )
| A. | 甲容器中的反应先达到化学平衡状态 | |
| B. | 两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量不相同 | |
| C. | 两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示 | |
| D. | 在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍 |
7.下列有关物质分类的正确组合是( )
| 分类组合 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | Na2CO3 | H2SO4 | NaHCO3 | SiO2 | CO2 |
| B | NaOH | HCl | NaCl | Na2O | CO |
| C | NaOH | CH3COOH | CaF2 | Na2O2 | SO2 |
| D | KOH | HNO3 | CaCO3 | CaO | SO3 |
| A. | A | B. | B | C. | C | D. | D |
11.120℃、101kPa时,两种气态烃的混合物2L完全燃烧,得到相同状况下3L CO2和3L水蒸气.这两种烃的可能组成是( )
| A. | CH4和C2H4 | B. | C2H6和C2H2 | C. | C3H8和C2H4 | D. | CH4和C2H2 |
7.下列化学变化中,相关示意图错误的是( )
| A. | 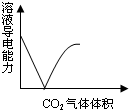 CO2通入澄清石灰水 | B. | 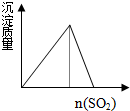 水玻璃中通入SO2 | ||
| C. | 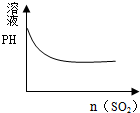 氯水中通入SO2 | D. | 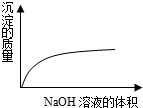 NaOH溶液滴入Ba(HCO3)2溶液 |
14.某学生设计如图实验步骤测定铁铜合金的组成:
说明:以上所有气体体积都已换算成标准状况时的数据
下列说法正确的是( )

说明:以上所有气体体积都已换算成标准状况时的数据
下列说法正确的是( )
| A. | 不溶物Y为Cu且质量是1.6g | |
| B. | 合金中铁单质的质量是1.68g | |
| C. | 合金中氧元素的物质的量是0.01mol | |
| D. | X溶液中既含有CuSO4又含有FeSO4 |
11.下列依据相关实验得出的结论正确的是( )
| A. | 向某溶液中加入氢氧化钠并加热,产生的气体能使湿润红色石蕊试纸变蓝,该溶液一定含NH4+ | |
| B. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| C. | 将某气体通入品红溶液中,红色褪去,该气体一定是SO2 | |
| D. | 向某溶液中加入盐酸酸化的BaCl2溶液有白色沉淀,该溶液中一定含有SO42- |
12.在相同条件下,把镁、铝、铁三种金属分别放入质量相等且足量的盐酸中,待反应完全后,三种溶液的质量相等,则投入的镁、铝、铁三种金属的质量关系是( )
| A. | Al>Mg>Fe | B. | Al=Mg=Fe | C. | Fe>Mg>Al | D. | Mg>Al>Fe |
