题目内容
下列各组微粒在指定的溶液中不能大量共存的是( )
| A、滴入KSCN溶液显红色的溶液中:K+、Fe2+、SO42-、Cl- |
| B、1mol?L-1的烧碱溶液中:O2、CO32-、SO42-、K+ |
| C、硫酸铜溶液中:Na+、Ba2+、NO3-、Cl- |
| D、含有大量HCO3-的澄清透明溶液中:K+、NO3-、Cl-、Na+ |
考点:离子共存问题
专题:离子反应专题
分析:A、滴入KSCN溶液显红色的溶液中存在铁离子,K+、Fe2+、SO42-、Cl-离子之间不反应,也不与铁离子反应;
B、烧碱为氢氧化钠,O2、CO32-、SO42-、K+离子之间不满足离子反应发生条件,且不与氢氧化钠溶液反应;
C、硫酸铜溶液中存在大量的硫酸根离子,钡离子能够与硫酸根离子反应生成硫酸钡沉淀;
D、K+、NO3-、Cl-、Na+离子之间不发生反应,也不与碳酸氢根离子反应,在溶液中能够共存.
B、烧碱为氢氧化钠,O2、CO32-、SO42-、K+离子之间不满足离子反应发生条件,且不与氢氧化钠溶液反应;
C、硫酸铜溶液中存在大量的硫酸根离子,钡离子能够与硫酸根离子反应生成硫酸钡沉淀;
D、K+、NO3-、Cl-、Na+离子之间不发生反应,也不与碳酸氢根离子反应,在溶液中能够共存.
解答:
解:A、该溶液中存在铁离子,K+、Fe2+、SO42-、Cl-离子之间不发生反应,且不与铁离子反应,在溶液中能够共存,故A错误;
B、该溶液中存在大量的氢氧根离子,O2、CO32-、SO42-、K+离子之间不发生反应,也不与NaOH液反应,在溶液中能够大量共存,故B错误;
C、Ba2+离子能够与SO42-反应生成硫酸钡沉淀,在溶液中不能大量共存,故C正确;
D、K+、NO3-、Cl-、Na+离子之间不满足离子反应条件,且不与HCO3-离子反应,在溶液中能够大量共存,故D错误;
故选C.
B、该溶液中存在大量的氢氧根离子,O2、CO32-、SO42-、K+离子之间不发生反应,也不与NaOH液反应,在溶液中能够大量共存,故B错误;
C、Ba2+离子能够与SO42-反应生成硫酸钡沉淀,在溶液中不能大量共存,故C正确;
D、K+、NO3-、Cl-、Na+离子之间不满足离子反应条件,且不与HCO3-离子反应,在溶液中能够大量共存,故D错误;
故选C.
点评:本题考查了离子共存的判断,题目难度中等,注意明确离子之间不能大量共存的条件,注意本题题干要求为溶液中“不能大量共存”,要求学生练掌握离子反应发生的条件.

练习册系列答案
相关题目
常温下,在0.1mol/L的碳酸钠溶液中,下列离子浓度的关系式正确的是( )
| A、2c(H2CO3)+c(HCO3-)+c(H+)═c(OH-) |
| B、c(Na+)═c(HCO3-)+c(H2CO3)+2c(CO32-) |
| C、c(Na+)>c(H+)>c(OH-)>c(CO32-) |
| D、c(Na+)+c(H+)═c(HCO3-)+c(OH-)+2c(CO32-) |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 利用此图装置可从氯化铁溶液中直接蒸发结晶获得氯化铁晶体 |
B、 利用此图装置可分离石油,得到汽油、煤油和柴油等各种馏分 |
C、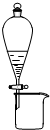 利用此图装置可分离CH3CH2OH和CH3COOC2H5混合液 |
D、 利用此图装置可进行酸碱中和滴定 |
NA为阿伏加德罗常数,下列说法正确的是( )
| A、NA个N2与0.5NA个H2物质的量之比为2:1 |
| B、标准状况下,11.2LBr2含有的原子数为NA |
| C、5.6L氯气和16.8L氧气的混合气体中所含的分子数一定为NA |
| D、1mol/LNaCl溶液中含有NA个氯离子 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下,11.2L乙醇所含的羟基数为0.5 NA |
| B、常温常压下,4.6g NO2和N2O4混合物中含有的原子总数为0.3 NA |
| C、1mol Cl2发生反应时,转移的电子数一定是2NA |
| D、常温下,1L pH=12的Ba(OH)2溶液中含有的OH-离子数为0.02NA |
 将洁净的三种金属片X、Y和Z分别放置在浸有食盐溶液的滤纸上并压紧(如图).每次实验时,电压表指针的偏移方向和读数如下表.已知构成两电极的金属,活泼性相差越大,则电压越大.对X、Y、Z和铜四种金属的下列说法,不正确的是( )
将洁净的三种金属片X、Y和Z分别放置在浸有食盐溶液的滤纸上并压紧(如图).每次实验时,电压表指针的偏移方向和读数如下表.已知构成两电极的金属,活泼性相差越大,则电压越大.对X、Y、Z和铜四种金属的下列说法,不正确的是( )| 金属片 | 电子流向 | 电压(V) |
| X | X→Cu | +0.78 |
| Y | Cu→Y | -0.15 |
| Z | Z→Cu | +1.35 |
| A、Z金属可作为牺牲阳极保护法的阳极,保护Y金属 |
| B、Y金属不能从硫酸溶液中置换出氢气 |
| C、三种金属的活泼性顺序为:Z>X>Y |
| D、X和Y能构成电压最大的原电池 |
 复方冬青油软膏具有强力迅速镇痛作用.其有效成分的分子模型如图.下列说法中不正确的是( )
复方冬青油软膏具有强力迅速镇痛作用.其有效成分的分子模型如图.下列说法中不正确的是( )| A、该有机物中含氧元素的质量分数最小 |
| B、该有机物分子中氢、氧原子的个数比为8:3 |
| C、该有机物完全燃烧生成二氧化碳和水 |
| D、该有机物的化学式为C8H8O3 |