题目内容
 复方冬青油软膏具有强力迅速镇痛作用.其有效成分的分子模型如图.下列说法中不正确的是( )
复方冬青油软膏具有强力迅速镇痛作用.其有效成分的分子模型如图.下列说法中不正确的是( )| A、该有机物中含氧元素的质量分数最小 |
| B、该有机物分子中氢、氧原子的个数比为8:3 |
| C、该有机物完全燃烧生成二氧化碳和水 |
| D、该有机物的化学式为C8H8O3 |
考点:球棍模型与比例模型,有机物的结构和性质
专题:有机化学基础
分析:由有机物的分子模型,确定分子构成,写出物质的化学式;根据物质的化学式或分子构成模型,判断该物质的分子中氢、氧原子个数比,推测生成物,计算组成元素的质量比,质量比中最小的元素即为物质中元素质量分数最小的元素.
解答:
解:由分子模型图可得知,该物质的分子由8个C原子、8个H原子、3个O原子构成,因此该有机物的化学式为C8H8O3,由化学式可知氢、氧原子的个数比为8:3,由化学式可知完全燃烧生成二氧化碳和水,故D、B、C正确;由化学式为C8H8O3可知在该有机物中三种元素质量之比为:12×8:8:16×3=12:1:6,故氢元素的质量分数最小,故A错误,
故选A.
故选A.
点评:本题考查了有机物结构和性质的关系,利用物质的分子模型图,正确认识物质的分子构成,并掌握有关化学式的意义,这样才能顺利完成本题的解答.

练习册系列答案
相关题目
下列各组微粒在指定的溶液中不能大量共存的是( )
| A、滴入KSCN溶液显红色的溶液中:K+、Fe2+、SO42-、Cl- |
| B、1mol?L-1的烧碱溶液中:O2、CO32-、SO42-、K+ |
| C、硫酸铜溶液中:Na+、Ba2+、NO3-、Cl- |
| D、含有大量HCO3-的澄清透明溶液中:K+、NO3-、Cl-、Na+ |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 装置可用于定量测定H2O2的分解速率 装置可用于定量测定H2O2的分解速率 |
B、 装置制备Fe(OH)2并能较长时间观察其颜色 装置制备Fe(OH)2并能较长时间观察其颜色 |
C、 装置测量Cu与浓硝酸反应产生气体的体积 装置测量Cu与浓硝酸反应产生气体的体积 |
D、 装置可用于蒸干NH4Cl饱和溶液制备NH4Cl晶体 装置可用于蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
下列反应中,离子方程式正确的是( )
| A、大理石溶于盐酸中:CO32-+2H+=CO2↑+H2O |
| B、AlCl3溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、硫酸镁溶液与氢氧化钡溶液混合:SO42-+Ba2+=BaSO4↓ |
| D、氯化铁溶液中加入铜片:Fe3++Cu=Fe2++Cu2+ |
设NA代表阿佛加德罗常数,下列说法正确的是( )
| A、22.4LCO和CO2的混合气体中所含的碳原子数一定是NA |
| B、含1mol HCl的盐酸溶液与足量Fe反应,Fe所失去的电子总数为2NA |
| C、常温常压下,32g O2和32g O3所含氧原子数都是2NA |
| D、标准状况下,11.2L H2O含有0.5NA分子 |
用下列有关实验装置进行相应实验,能达到实验目的是( )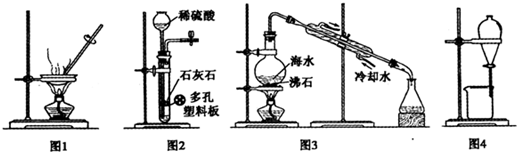

| A、用图1装置蒸干CuCl2饱和溶液制备CuCl2晶体 |
| B、用图2装置制取二氧化碳气体 |
| C、用图3装置蒸馏海水制取少量淡水 |
| D、用图4装置分离乙醇与乙酸乙酯的混合物 |


