题目内容
9.将0.02molCl2缓缓通入含0.1molH2SO3和0.02molHBr的混合液中,在此过程溶液的c(H+)与Cl2用量的关系示意图是(溶液的体积均视为不变)( )| A. | 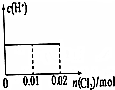 | B. |  | C. | 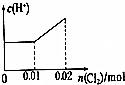 | D. |  |
分析 根据方程式知,还原性H2SO3>HBr,所以向混合溶液中通入氯气时,先氧化H2SO3后氧化HBr,根据方程式H2SO3+Cl2+H2O═2HCl+H2SO4知,0.01mol H2SO3完全被氧化,需要n(Cl2)=n(H2SO3)=0.01mol,
亚硫酸是弱酸、盐酸和硫酸都是强酸,所以随着反应的进行氢离子浓度增大;
剩余的0.01mol氯气氧化HBr,根据Cl2+2HBr=Br2+2HCl知,0.01mol氯气能氧化0.02molHBr,HCl、HBr都是强电解质,溶液中c(H+)不变.
解答 解:根据方程式知,还原性H2SO3>HBr,所以向混合溶液中通入氯气时,先氧化H2SO3后氧化HBr,根据方程式H2SO3+Cl2+H2O═2HCl+H2SO4知,0.01mol H2SO3完全被氧化,需要n(Cl2)=n(H2SO3)=0.01mol,亚硫酸是弱酸、盐酸和硫酸都是强酸,所以随着反应的进行氢离子浓度增大;
剩余的0.01mol氯气氧化HBr,根据Cl2+2HBr=Br2+2HCl知,0.01mol氯气能氧化0.02molHBr,HCl、HBr都是强电解质,所以该过程中氢离子浓度不变,即横坐标增大而纵坐标不变,
故选D.
点评 本题以物质之间的反应为载体考查氧化还原反应的计算、强弱电解质等知识点,明确方程式中各个物理量之间的关系是解本题关键,注意氯气和HBr反应时氢离子浓度不变,为易错点.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
19.下列措施符合安全要求的是( )
| A. | 金属钠着火时,立即用沾水的毛巾覆盖 | |
| B. | 将含有硫酸的废液倒人水池,用大量水冲人下水道 | |
| C. | 锌和稀硫酸反应生成的氢气可直接点燃,观察火焰的颜色 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 |
20.下列实验室除杂所用试剂和操作均合理的是( )
| 选项 | 物质(括号中为杂质) | 除杂试剂 | 操作 |
| A | 铁器(植物油) | 热纯碱溶液 | 洗涤 |
| B | BaCO3(BaSO${\;}_{{4}_{\;}}$) | 饱和碳酸钠溶液 | 搅拌、过滤 |
| C | KNO3(NaCl) | 水 | 蒸发结晶 |
| D | HCl(Cl2) | 饱和食盐水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
17.NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| B. | Na2O2与CO2反应生成11.2LO2(标准状况),反应中转移的电子数为2NA | |
| C. | 在标准状况下,22.4LSO3所含的氧原子数目为3NA | |
| D. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
4.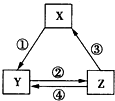 下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )
 下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )| 选项 | X | Y | Z |
| A | Mg | MgO | MgCl2 |
| B | Fe | FeCl3 | FeCl2 |
| C | Na2CO3 | NaOH | NaHCO3 |
| D | Cl2 | Ca(ClO)2 | HClO |
| A. | A | B. | B | C. | C | D. | D |
14.已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且产物的成分与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是( )
| A. | 某温度下,反应后c(Cl-):c(ClO-)=6,则溶液中c(ClO-):c(ClO3-)=1 | |
| B. | 参加反应的氯气的物质的量等于0.5amol | |
| C. | 改变温度,反应中转移电子的物质的量n的范围:$\frac{1}{2}$amol<n<$\frac{5}{6}$amol | |
| D. | 改变温度,产物中KClO3的最大理论产量为$\frac{1}{6}$amol |
1.江苏省将大力实施“清水蓝天”工程.下列不利于“清水蓝天”工程实施的是( )
| A. | 大力实施矿物燃料“脱硫、脱销技术”,减少硫的氧化物和氮的氧化物污染 | |
| B. | 禁止未经处理的工业废水和生活污水的任意排放 | |
| C. | 积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用 | |
| D. | 大量使用化肥农药,提高粮食产量 |
18.某校化学兴趣小组的学生,分成两组对酸雨及空气中二氧化硫的含量进行了测定.第一组,取刚降到地面的酸雨水样,进行了如下实验:
①将一片红色的玫瑰花瓣浸在一份水样中;
②向雨水试样中滴加氯化钡溶液,有白色沉淀生成;
③每隔一定时间测定其pH,数据如表Ⅰ所示.
表Ⅰ不同时间酸雨的pH
(1)一段时间后,观察到玫瑰花瓣红色变浅,原因是SO2有漂白作用.
(2)生成白色沉淀的离子方程式Ba2++SO42-=BaSO4↓.
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示)2SO2+2H2O+O2=2H2SO4.
第二组,拟用如图装置定量分析空气中SO2的含量:

(4)通入空气前应进行的实验操作是气密性检查;KMnO4溶液中导管末端做成球状多孔结构的作用是增大接触面积,有利于SO2的充分吸收.
(5)已知:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+.随着空气的不断通入,酸性高锰酸钾的溶液逐渐变浅直至褪色,说明SO2具有还原性性.
(6)若实验中气体流速aL•min-1,酸性KMnO4溶液的体积bL,其浓度为cmol•L-1,从气体通入到紫色恰好褪去,用时5min.则空气中二氧化硫的含量为$\frac{32bc}{a}$g•L-1.
①将一片红色的玫瑰花瓣浸在一份水样中;
②向雨水试样中滴加氯化钡溶液,有白色沉淀生成;
③每隔一定时间测定其pH,数据如表Ⅰ所示.
表Ⅰ不同时间酸雨的pH
| 测定时间/小时钟 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
(2)生成白色沉淀的离子方程式Ba2++SO42-=BaSO4↓.
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示)2SO2+2H2O+O2=2H2SO4.
第二组,拟用如图装置定量分析空气中SO2的含量:

(4)通入空气前应进行的实验操作是气密性检查;KMnO4溶液中导管末端做成球状多孔结构的作用是增大接触面积,有利于SO2的充分吸收.
(5)已知:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+.随着空气的不断通入,酸性高锰酸钾的溶液逐渐变浅直至褪色,说明SO2具有还原性性.
(6)若实验中气体流速aL•min-1,酸性KMnO4溶液的体积bL,其浓度为cmol•L-1,从气体通入到紫色恰好褪去,用时5min.则空气中二氧化硫的含量为$\frac{32bc}{a}$g•L-1.
19.在一定温度时,N2与H2反应过程中能量变化的曲线如图,下列叙述正确的是( )

| A. | 该反应的热化学方程式为:N2+3H2?2NH3△H=-92KJ/mol | |
| B. | a曲线是加人催化剂时的能量变化曲线 | |
| C. | 加人催化剂,该化学反应的放热减少 | |
| D. | 反应物的总能量高于生成物的总能量 |