题目内容
15.某硝酸盐M(NO3)2热分解化学方程式为:2M(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2MO+4NO2↑+O2↑,加热18.8gM(NO3)2使其完全分解,共收集5.6L气体(标准状况下),则M摩尔质量为( )
| A. | 64 g•mol-1 | B. | 24 g•mol-1 | C. | 56 g•mol-1 | D. | 188 g•mol-1 |
分析 根据n=$\frac{V}{{V}_{m}}$计算混合气体的物质的量,根据方程式化学计量数关系计算出18.8g M(NO3)2的物质的量,根据M=$\frac{m}{M}$计算出摩尔质量,进而计算M的摩尔质量.
解答 解:在标准状况下收集气体体积为5.6L,物质的量为:$\frac{5.6L}{22.4L/mol}$mol=0.25mol,
根据反应方程式2M(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2MO+4NO2↑+O2↑,可知2molM(NO3)2分解生成5mol气体,
故M(NO3)2的物质的量为:0.25mol×$\frac{2}{4+1}$=0.1mol,M(NO3)2的摩尔质量为:$\frac{18.8g}{0.1mol}$=188g/mol,
所以M的摩尔质量为:188g/mol-2×62g/mol=64g/mol,
故选A.
点评 本题考查化学方程式的有关计算、摩尔质量等,难度不大,注意理解掌握摩尔质量的常用计算方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.化学实验室中常将溶液或试剂进行酸化,下列酸化处理正确的是( )
| A. | 检验氯乙烷中的氯元素,加碱溶液加热后,用稀硫酸酸化后,再检验 | |
| B. | 鉴别溶液中是否有SO42-,用盐酸酸化 | |
| C. | 为抑制Fe2+的水解,用稀硝酸酸化 | |
| D. | 为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化 |
6.空气污染指数(API)与空气质量等级关系可以用下图表示.

下表是某城市某日空气质量报告
(1)表中的PM10指的是可吸入颗粒物
(2)某日该城市市区各项污染物污染指数分别为:SO2-58,NO2-21,PM10-23,则当日首要污染物为二氧化硫(SO2),空气质量级别为良(选填“轻微污染”、“良”、“优”)
(3)空气中硫的氧化物和氮的氧化物随雨水降下,反应生成酸,当雨水的pH<(选填“>”、“<”、“=”)5.6时,称之为酸雨.现有一份雨水样品,每隔一段时间测定该样品的pH,发现随着时间的推移,pH将变小(选填“变大”、“变小”、“不变”).
(4)我国是燃煤大国,现测得某燃煤样品中含硫质量分数为0.032%,燃烧1吨该燃煤,理论上可生成SO222.4L(标准状况)(S+O2═SO2,S的摩尔质量为32g/mol).请你提出一种治理酸雨的措施使用清洁能源、燃煤脱硫等.

下表是某城市某日空气质量报告
| 污 染 指 数 | 首要 污染物 | 空气 质量等级 | ||
| SO2 | NO2 | PM10 | ||
| 23 | 35 | 56 | PM10 | 良 |
(2)某日该城市市区各项污染物污染指数分别为:SO2-58,NO2-21,PM10-23,则当日首要污染物为二氧化硫(SO2),空气质量级别为良(选填“轻微污染”、“良”、“优”)
(3)空气中硫的氧化物和氮的氧化物随雨水降下,反应生成酸,当雨水的pH<(选填“>”、“<”、“=”)5.6时,称之为酸雨.现有一份雨水样品,每隔一段时间测定该样品的pH,发现随着时间的推移,pH将变小(选填“变大”、“变小”、“不变”).
(4)我国是燃煤大国,现测得某燃煤样品中含硫质量分数为0.032%,燃烧1吨该燃煤,理论上可生成SO222.4L(标准状况)(S+O2═SO2,S的摩尔质量为32g/mol).请你提出一种治理酸雨的措施使用清洁能源、燃煤脱硫等.
3.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L CCl4所含原子数目为2.5NA | |
| B. | 常温常压下,64g SO2中含有的原子数为3NA | |
| C. | 将1 mol Cl2通入水中能生成1mol HClO | |
| D. | 2L 0.1 mol•L-1K2SO4溶液中含K+物质的量为0.2 mol |
10.下列物质与水反应能生成强酸的是( )
| A. | Cl2 | B. | Na2O | C. | CO2 | D. | NH3 |
9.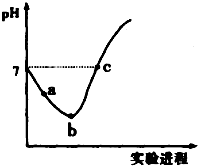 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol•L-1 的NaOH 溶液,整个实验进程中溶液的pH 变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol•L-1 的NaOH 溶液,整个实验进程中溶液的pH 变化曲线如图所示,下列叙述正确的是( )
 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol•L-1 的NaOH 溶液,整个实验进程中溶液的pH 变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol•L-1 的NaOH 溶液,整个实验进程中溶液的pH 变化曲线如图所示,下列叙述正确的是( )| A. | 向a 点所示溶液中通入SO2,溶液的酸性和漂白性均增强 | |
| B. | b 点所示的溶液中:c(H+)>c(Cl-)>c(ClO-)>c(HClO) | |
| C. | 由a 点到b 点的过程中,溶液中$\frac{c({H}^{+})}{c(Cl{O}^{-})}$ 减小 | |
| D. | c 点所示溶液中:c(Na+ )=2c(ClO-)+c(HClO) |
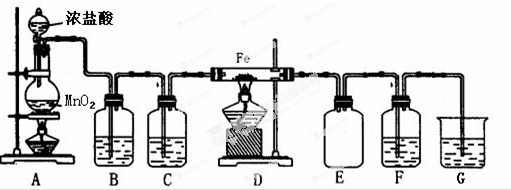
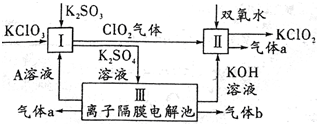 氯酸钾(KC1O3)和亚氯酸钾(KClO2)可以相互转化,KClO2在碱性环境中能稳定存在,生产KClO2的主要流程如图所示.
氯酸钾(KC1O3)和亚氯酸钾(KClO2)可以相互转化,KClO2在碱性环境中能稳定存在,生产KClO2的主要流程如图所示.