题目内容
16.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )| A. | 107 g Fe(OH)3胶体中胶体粒子的数目为NA | |
| B. | 2molSO2与1molO2反应生成的SO3分子数为2NA | |
| C. | 14g分子式为CnH2n的链烃中含有的碳碳双键的数目为$\frac{{N}_{A}}{n}$ | |
| D. | 7.8 g Na2O2与足量水反应转移的电子散为0.2NA |
分析 A.氢氧化铁胶体粒子是氢氧化铁的集合体;
B.二氧化硫与氧气反应生成三氧化硫为可逆反应,依据可逆反应不能进行到底的特点解答;
C.分子式为CnH2n的链烃为单烯烃;
D.Na2O2与足量水反应,过氧化钠既是氧化剂又是还原剂,所以1mol Na2O2与足量水反应转移的电子的物质的量为1mol.
解答 解:A.氢氧化铁胶体粒子是氢氧化铁的集合体,NA个Fe(OH)3胶体粒子的质量大于107g,故A错误;
B.二氧化硫与氧气反应生成三氧化硫为可逆反应,可逆反应不能进行到底,所以2molSO2与1molO2反应生成的SO3分子数小于2NA,故B错误;
C.分子式为CnH2n的链烃为单烯烃,最简式为CH2,14g分子式为CnH2n的链烃中含有的碳碳双键的数目为=$\frac{14g}{14ng/mol}$×NA=$\frac{{N}_{A}}{n}$,故C正确;
D.Na2O2与足量水反应,过氧化钠既是氧化剂又是还原剂,所以1mol Na2O2与足量水反应转移的电子的物质的量为1mol,所以0.1mol Na2O2与足量水反应转移的电子的物质的量为0.1mol,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要考查质量换算物质的量计算微粒数,明确胶体、过氧化钠、有机物结构组成是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6. 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
(1)①由上表数据可知该反应为放热 (填放热,吸热,无法确定 )反应.
②下列措施能用勒夏特列原理解释是ad.(填序号)
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500°C左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol氨气溶于水后再与含有0.2mol硫酸的溶液反应放热QkJ,请你用热化学方程式表示其反应
式NH3.H2O(aq)+H2SO4(aq)=NH4HSO4(aq)+H2O(l)△H=-5Q kJ•mol-1.
(3)常温时,将amol氨气溶于水后,再通入bmol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl-),则一水合
氨的电离平衡常数Kb=$\frac{1{0}^{-7}b}{a-b}$.(用ab表示)
(4)原料气H2可通过反应 CH4(g)+H2O (g)?CO(g)+3H2(g) 获取,已知该反应中,当初始混合气
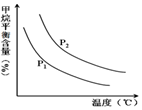
中的$\frac{n({H}_{2}O)}{n(C{H}_{4})}$恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2
(填“>”、“=”或“<”).
②其它条件一定,升高温度,氢气的产率会增大.(填“增大”,“减小”减小,“不变”不变)
(5)原料气H2还可通过反应CO(g)+H2O(g)?CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,该温度下反应的平衡常数K值为2.25.
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变 b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
②下列措施能用勒夏特列原理解释是ad.(填序号)
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500°C左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol氨气溶于水后再与含有0.2mol硫酸的溶液反应放热QkJ,请你用热化学方程式表示其反应
式NH3.H2O(aq)+H2SO4(aq)=NH4HSO4(aq)+H2O(l)△H=-5Q kJ•mol-1.
(3)常温时,将amol氨气溶于水后,再通入bmol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl-),则一水合
氨的电离平衡常数Kb=$\frac{1{0}^{-7}b}{a-b}$.(用ab表示)
(4)原料气H2可通过反应 CH4(g)+H2O (g)?CO(g)+3H2(g) 获取,已知该反应中,当初始混合气
中的$\frac{n({H}_{2}O)}{n(C{H}_{4})}$恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2
(填“>”、“=”或“<”).
②其它条件一定,升高温度,氢气的产率会增大.(填“增大”,“减小”减小,“不变”不变)
(5)原料气H2还可通过反应CO(g)+H2O(g)?CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,该温度下反应的平衡常数K值为2.25.
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变 b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.
7.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 80 mL10 mol/L的浓盐酸与足量MnO2反应,转移电子数为0.4 NA | |
| B. | 通入了1 mol Cl2的新制氯水中,HC1O、Cl-、C1O-粒子数之和为2NA | |
| C. | 1 mol Na2O2中含有的阴离子数为2 NA | |
| D. | 标准状况下,4.48L NH3中共用电子对数为0.6 NA |
4.如图为二维平面晶体示意图,对a、b晶体示意图所表示的化学式说法正确的是( )

| A. | a为A2X3,b为AX3 | B. | a为AX3,b为AX2 | C. | a为AX2,b为AX3 | D. | a为AX3,b为A2X3 |
11.下列关于有机化合物的说法正确的是( )
| A. | 乙醇的水溶液俗称酒精 | |
| B. | 由苯与氯气在一定条件下生成C6H6Cl6的反应属于取代反应 | |
| C. | 化学式为C4H10O的饱和一元醇有4种 | |
| D. | 糖类发生水解反应的最终产物都是葡萄糖 |
1.氧、硅、铝是地壳中含量最多的三种元素,下列叙述正确的是( )
| A. | 普通玻璃、水泥成分中都含有这三种元素 | |
| B. | 自然界中存在单质硅 | |
| C. | 氧元素与另外两种元素形成的二元化合物都能与NaOH的浓溶液反应 | |
| D. | 电解熔融状态的SiO2和A12O3可以制得Si、A1,且都有氧气生成 |
8.如图为生锈了的家用铁锅,下列有关解释事实的方程式不正确的是( )


| A. | 铁锅生锈过程中有原电池反应,负极反应式是:Fe-2e-=Fe2+ | |
| B. | 铁锅生锈过程中有Fe(OH)3生成:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 摄入体内的铁锈会在胃内产生不利于健康的Fe3+:Fe2O3+6H+═2Fe3++3H2O | |
| D. | 用醋可除去铁锈:6CH3COOH+Fe2O3═6CH3COO-+2Fe3++3H2O |
12.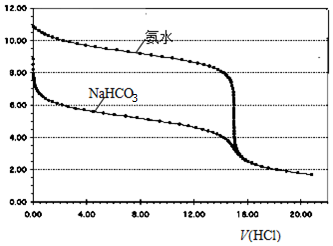 常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )
常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )
 常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )
常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )| A. | 当V(HCl)=0 mL时,c(NH3•H2O)=c(HCO3-) | |
| B. | 当V(HCl)=4.00 mL时,c(NH4+)>c(NH3•H2O)>c(HCO3-)>c(CO32-) | |
| C. | 当V(HCl)=8.00 mL时,c(Na+)<c(NH4+)+c(HCO3-)+2c(CO32-) | |
| D. | 当V(HCl)=15.00 mL时,c(Na+)=c(NH4+)+c(NH3•H2O) |
13.仪器名称为“分液漏斗”的是( )
| A. |  | B. |  | C. |  | D. |  |