题目内容
4.如图为二维平面晶体示意图,对a、b晶体示意图所表示的化学式说法正确的是( )
| A. | a为A2X3,b为AX3 | B. | a为AX3,b为AX2 | C. | a为AX2,b为AX3 | D. | a为AX3,b为A2X3 |
分析 由图中直接相邻的原子数可以求出a、b中两类原子数目之比,据此确定.
解答 解:a图中每个斜线球周围有6个白色球,而每个白色球为3个斜线球共有,故斜线球与白色球数目之比=1:6×$\frac{1}{3}$=1:2,a的化学式为AX2;
b图中每个斜线球周围有6个白色球,而每个白色球为2个斜线球共有,故斜线球与白色球数目之比=1:6×$\frac{1}{2}$=1:3,b的化学式为AX3;
故选C.
点评 本题考查了根据晶体图来确定化学式,题目难度不大,属于基础性知识的考查,注意应用均摊法计算,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
15.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 78gNa2O2固体中阴离子的个数为2NA | |
| B. | Na2O2与H2O反应生成1.12L(标准状况)气体,反应中转移的电子数为0.2NA | |
| C. | 1mol氯气溶于足量水中,转移的电子数为NA | |
| D. | 在1 L0.1mol/L碳酸钠溶液中,阴离子总数大于0.1NA |
12.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,2.24 LC2H4和C2H2的混合气体中含碳原子数目小于0.2 NA | |
| B. | 100 mL 1.0 mol/L FeCl3溶液与足量Cu反应,转移的电子数为0.2 NA | |
| C. | 标况下44.8 mL氯气通入足量水中发生反应,转移电子数为2×10-3NA | |
| D. | 常温下,pH=2的H2SO4溶液中含有的H+数目为0.02 NA |
19.下列各组离子不可能大量共存的是( )
| A. | 与铝反应放出氢气的溶液中:Na+、Cl-、S2-、SO32- | |
| B. | c(HCO3-)=0.1mol•L-1的溶液中:Na+、K+、CO32-、Br- | |
| C. | 在由水电离出的c(OH-)=10-18 mol•L-1的溶液中Na+、Mg2+、NO3-、I- | |
| D. | 在能使pH试纸变深蓝色的溶液中:Na+、S2-、CO32-、NO3-、 |
9.化学与生活密切相关,下列有关说法错误的是( )
| A. | Cu2+为重金属离子,故CuSO4不能用于生活用水消毒 | |
| B. | 卤水煮豆腐是Mg2+、Ca2+等使蛋白质胶体发生凝聚过程 | |
| C. | 纯碱溶液可以洗涤餐具上的油渍 | |
| D. | 油漆刷在钢铁护栏表层用来防止金属锈蚀 |
16.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 107 g Fe(OH)3胶体中胶体粒子的数目为NA | |
| B. | 2molSO2与1molO2反应生成的SO3分子数为2NA | |
| C. | 14g分子式为CnH2n的链烃中含有的碳碳双键的数目为$\frac{{N}_{A}}{n}$ | |
| D. | 7.8 g Na2O2与足量水反应转移的电子散为0.2NA |
13.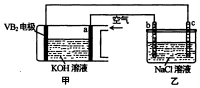 碱性硼化钒--空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5,室温下用该电池为电源,用惰性电极电解饱和氯化钠溶液,装置如图.当外电路中通过0.04mol电子时,乙装置中溶液的体积为400mL.则下列说法正确的是( )
碱性硼化钒--空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5,室温下用该电池为电源,用惰性电极电解饱和氯化钠溶液,装置如图.当外电路中通过0.04mol电子时,乙装置中溶液的体积为400mL.则下列说法正确的是( )
 碱性硼化钒--空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5,室温下用该电池为电源,用惰性电极电解饱和氯化钠溶液,装置如图.当外电路中通过0.04mol电子时,乙装置中溶液的体积为400mL.则下列说法正确的是( )
碱性硼化钒--空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5,室温下用该电池为电源,用惰性电极电解饱和氯化钠溶液,装置如图.当外电路中通过0.04mol电子时,乙装置中溶液的体积为400mL.则下列说法正确的是( )| A. | 外电路中电子由a电极流向b电极 | |
| B. | 电极上生成气体的体积为4.48L | |
| C. | 乙装置中溶液的pH为13 | |
| D. | VB2电极发生的电极反应为:VB2+11H2O-22e-=VB2+2B2O3+22H+ |
1.分子式为C5H12O且含有2个甲基(-CH3)的有机化合物共有(不考虑立体异构)( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
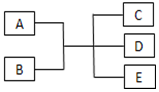 已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如图反应关系.
已知A、B、C、D、E是化学中常见的物质,常温下,E是一种无色无味的液体,它们之间有如图反应关系.