题目内容
工业上从煤干馏粗产品煤焦油中可以分离出萘,以萘为主要原料合成除草剂敌草胺的流程图如下:
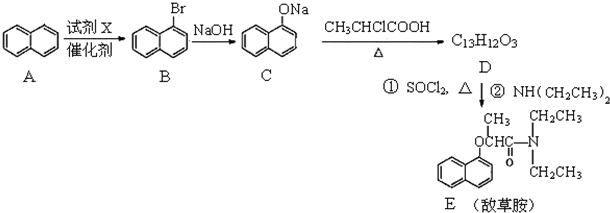
(1)试剂X是 ;A生成B时,有另一种一溴代物副产物,它的结构简式为 ;
(2)D的结构简式为 ;
(3)写出同时满足下列条件的D的一种同分异构体的结构简式: .
①是A的衍生物,且取代基都在同一个苯环上;
②能与金属钠反应放出H2,遇氯化铁溶液不显紫色;
③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氢原子.
(4)已知:RCH2COOH
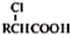 ,写出以苯酚、乙醇和乙酸为原料制备
,写出以苯酚、乙醇和乙酸为原料制备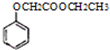 的合成路线流程图(无机试剂任用).合成路线流程图例如下:
的合成路线流程图(无机试剂任用).合成路线流程图例如下:
H2C=CH2
CH3CH2Br
CH3CH2OH.

(1)试剂X是
(2)D的结构简式为
(3)写出同时满足下列条件的D的一种同分异构体的结构简式:
①是A的衍生物,且取代基都在同一个苯环上;
②能与金属钠反应放出H2,遇氯化铁溶液不显紫色;
③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氢原子.
(4)已知:RCH2COOH
| PCI3 |
| △ |
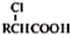 ,写出以苯酚、乙醇和乙酸为原料制备
,写出以苯酚、乙醇和乙酸为原料制备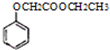 的合成路线流程图(无机试剂任用).合成路线流程图例如下:
的合成路线流程图(无机试剂任用).合成路线流程图例如下:H2C=CH2
| HBr |
| NaOH溶液 |
| △ |
考点:有机物的合成
专题:有机物的化学性质及推断
分析:(1)对比A、B的结构可知,A生成B为苯环上发生取代反应,可知X为液溴,而-Br也可发生2号碳位上取代反应;
(2)对比D的分子式、NH(CH2CH3)2与E的结构,可以确定D的结构简式为 ;
;
(3)D的同分异构体符合:①是A的衍生物,且取代基都在同一个苯环上;
②能与金属钠反应放出H2,遇氯化铁溶液不显紫色,不含酚羟基;
③可发生水解反应,其中一种水解产物能发生银镜反应,具有甲酸形成的酯基,结合②可知,还含有醇羟基,而另一种水解产物分子中有5种不同化学环境的氢原子,不可能有一个支链,结合D的结构可知,应含有2个相同的取代基-CH2OH,处于同一苯环中1,4位置或2,3位置;
(4)由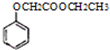 可知,应先制备
可知,应先制备 ,再与乙醇发生酯化反应,根据转化关系中C→D的转化可知,苯酚钠与ClCH2COOH反应得到
,再与乙醇发生酯化反应,根据转化关系中C→D的转化可知,苯酚钠与ClCH2COOH反应得到 ,苯酚与氢氧化钠反应得到苯酚钠,由信息可知CH3COOH在PCl3、加热条件下可以得到ClCH2COOH.
,苯酚与氢氧化钠反应得到苯酚钠,由信息可知CH3COOH在PCl3、加热条件下可以得到ClCH2COOH.
(2)对比D的分子式、NH(CH2CH3)2与E的结构,可以确定D的结构简式为
 ;
;(3)D的同分异构体符合:①是A的衍生物,且取代基都在同一个苯环上;
②能与金属钠反应放出H2,遇氯化铁溶液不显紫色,不含酚羟基;
③可发生水解反应,其中一种水解产物能发生银镜反应,具有甲酸形成的酯基,结合②可知,还含有醇羟基,而另一种水解产物分子中有5种不同化学环境的氢原子,不可能有一个支链,结合D的结构可知,应含有2个相同的取代基-CH2OH,处于同一苯环中1,4位置或2,3位置;
(4)由
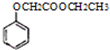 可知,应先制备
可知,应先制备 ,再与乙醇发生酯化反应,根据转化关系中C→D的转化可知,苯酚钠与ClCH2COOH反应得到
,再与乙醇发生酯化反应,根据转化关系中C→D的转化可知,苯酚钠与ClCH2COOH反应得到 ,苯酚与氢氧化钠反应得到苯酚钠,由信息可知CH3COOH在PCl3、加热条件下可以得到ClCH2COOH.
,苯酚与氢氧化钠反应得到苯酚钠,由信息可知CH3COOH在PCl3、加热条件下可以得到ClCH2COOH.解答:
解:(1)对比A、B的结构可知,A生成B为苯环上发生取代反应,可知X为液溴,而-Br也可发生2号碳上取代反应,则副产物为 ,故答案为:液溴;
,故答案为:液溴; ;
;
(2)对比D的分子式、NH(CH2CH3)2与E的结构,可以确定D的结构简式为 ,故答案为:
,故答案为: ;
;
(3)D的同分异构体符合:①是A的衍生物,且取代基都在同一个苯环上;
②能与金属钠反应放出H2,遇氯化铁溶液不显紫色,不含酚羟基;
③可发生水解反应,其中一种水解产物能发生银镜反应,具有甲酸形成的酯基,结合②可知,还含有醇羟基,而另一种水解产物分子中有5种不同化学环境的氢原子,不可能有一个支链,结合D的结构可知,应含有2个相同的取代基-CH2OH,处于同一苯环中1,4位置或2,3位置,
符合条件的同分异构体为: ,
,
故答案为: ;
;
(4)由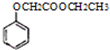 可知,应先制备
可知,应先制备 ,再与乙醇发生酯化反应,根据转化关系中C→D的转化可知,苯酚钠与ClCH2COOH反应得到
,再与乙醇发生酯化反应,根据转化关系中C→D的转化可知,苯酚钠与ClCH2COOH反应得到 ,则苯酚与氢氧化钠反应得到苯酚钠,由信息可知CH3COOH在PCl3、加热条件下可以得到ClCH2COOH,故合成路线图为:
,则苯酚与氢氧化钠反应得到苯酚钠,由信息可知CH3COOH在PCl3、加热条件下可以得到ClCH2COOH,故合成路线图为: ,
,
故答案为: .
.
 ,故答案为:液溴;
,故答案为:液溴; ;
;(2)对比D的分子式、NH(CH2CH3)2与E的结构,可以确定D的结构简式为
 ,故答案为:
,故答案为: ;
;(3)D的同分异构体符合:①是A的衍生物,且取代基都在同一个苯环上;
②能与金属钠反应放出H2,遇氯化铁溶液不显紫色,不含酚羟基;
③可发生水解反应,其中一种水解产物能发生银镜反应,具有甲酸形成的酯基,结合②可知,还含有醇羟基,而另一种水解产物分子中有5种不同化学环境的氢原子,不可能有一个支链,结合D的结构可知,应含有2个相同的取代基-CH2OH,处于同一苯环中1,4位置或2,3位置,
符合条件的同分异构体为:
 ,
,故答案为:
 ;
;(4)由
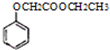 可知,应先制备
可知,应先制备 ,再与乙醇发生酯化反应,根据转化关系中C→D的转化可知,苯酚钠与ClCH2COOH反应得到
,再与乙醇发生酯化反应,根据转化关系中C→D的转化可知,苯酚钠与ClCH2COOH反应得到 ,则苯酚与氢氧化钠反应得到苯酚钠,由信息可知CH3COOH在PCl3、加热条件下可以得到ClCH2COOH,故合成路线图为:
,则苯酚与氢氧化钠反应得到苯酚钠,由信息可知CH3COOH在PCl3、加热条件下可以得到ClCH2COOH,故合成路线图为: ,
,故答案为:
 .
.
点评:本题考查有机物的合成,侧重考查学生分析推理能力,充分利用有机物的结构进行分析解答,是对有机化学基础的综合考查,(4)中合成路线充分利用题目中转化关系设计,难度中等.

练习册系列答案
相关题目
已知BaCO3和BaSO4溶度积常数分别为KSP=5.1×10-4,KSP=1.1×10-10,则BaSO4可作钡餐,BaCO3不可作钡餐的主要理由是( )
| A、BaSO4的溶度积常数比BaCO3的小 |
| B、SO42-没有毒性CO32-有毒性 |
| C、BaSO4密度大 |
| D、胃酸能与CO32-结合,生成CO2和H2O,使BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大,造成中毒 |




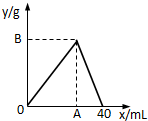 如图是表示往50mL AlCl3溶液中滴加4mol?L-1的NaOH溶液,生成沉淀的质量(y轴)与消耗NaOH溶液的体积(x轴)的关系.填空:
如图是表示往50mL AlCl3溶液中滴加4mol?L-1的NaOH溶液,生成沉淀的质量(y轴)与消耗NaOH溶液的体积(x轴)的关系.填空: