题目内容
1.一定量的某饱和一元醛发生银镜反应可得10.8g银,将等量的该醛完全燃烧,生成2.7g水.此醛可能是( )| A. | 乙醛 | B. | 丙醛 | C. | 丁醛 | D. | 戊醛 |
分析 若为甲醛,则HCHO~4Ag,选项中无甲醛,饱和一元醛的通式是CnH2nO,根据关系式R-CHO~2Ag计算醛的物质的量,根据H原子守恒计算醛中H原子数目,再结合组成通式可确定醛的分子式.
解答 解:21.6g Ag的物质的量为$\frac{10.8g}{108g/mol}$=0.1mol,醛燃烧生成水的物质的量为$\frac{2.7g}{18g/mol}$=0.15mol,
设饱和一元醛的通式是CnH2nO,由R-CHO~2Ag可知,醛的物质的量为0.1mol×$\frac{1}{2}$=0.05mol,由H原子守恒可知醛中H原子数目为$\frac{0.15mol×2}{0.05mol}$=6,
A为CH3CHO,B为CH3CH2CHO,C为CH3CH2CH2CHO,D为CH3CH2CH2CH2CHO,
故选B.
点评 本题考查有机反应的计算,为高频考点,把握-CHO与Ag的关系及H原子守恒为解答的关键,侧重分析与计算能力的考查,注意原子守恒法的应用,题目难度不大.

练习册系列答案
相关题目
11.下列说法正确的是( )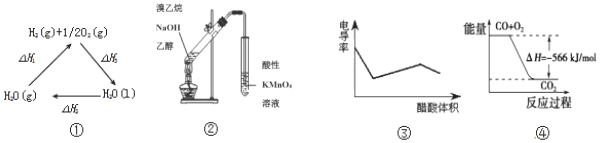

| A. | 图①中△H1=△H2+△H3 | |
| B. | 图②可用于证明实验中生成了乙烯 | |
| C. | 图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 | |
| D. | 图④可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量 |
12.有下列几种方法制备O2:(l)KClO3和MnO2共热,(2)H2O2中加MnO2,(3)KMnO4受热分解,(4)Na2O2和水,若要制相同质量的O2,则上述反应中相关物质转移的电子数之比为( )
| A. | 3:2:4:1 | B. | 1:1:1:1 | C. | 2:1:2:1 | D. | 1:2:1:2 |
9.二氯化硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构与类似H2O2.常温下S2Cl2是一种橙黄色的液体,可与水反应,产生能使品红褪色的气体.下列说法错误的是( )
| A. | S2Cl2的结构式为Cl-S-S-Cl | |
| B. | S2Cl2中S原子的杂化类型为sp2杂化 | |
| C. | S2Cl2分子中各原子核外最外层电子均达到8电子稳定结构 | |
| D. | S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
6.下列说法正确的是( )
| A. | 二氧化硫可用于杀菌、消毒 | |
| B. | 煤经过气化和液化等物理变化可转化为清洁能源 | |
| C. | 氯气和明矾均可做自来水的消毒剂 | |
| D. | 食品保鲜剂中所含铁粉和生石灰均作还原剂 |
13.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2LCH3Cl含极性共价键数目为2NA | |
| B. | 0.1L 1.0mol/L Na2S溶液中S2-和HS-总数为0.1NA | |
| C. | 22.4g 铁粉与稀硝酸完全反应时转移的电子数一定为1.2NA | |
| D. | 常温常压下,16g14CH4中所含电子数目为8NA |
 ,试回答下列问题:
,试回答下列问题: