题目内容
14.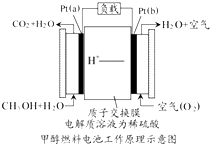 科学家预言,燃料电池将是21世纪获得电能的重要途径,近几年开发甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过,其工作原理的示意图如下:
科学家预言,燃料电池将是21世纪获得电能的重要途径,近几年开发甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过,其工作原理的示意图如下:(1)Pt(a)电极是电池的负极,电极反应式为CH3OH+H2O-6e-═CO2+6H+;Pt(b)电极发生还原反应(填“氧化”或“还原”),电极反应式为O2+4H++4e-═2H2O.
(2)电池的总反应方程式为2CH3OH+3O2=2CO2+4H2O.
(3)如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有$\frac{1}{3}$mol.
分析 (1)该原电池中质子交换膜只允许质子和水分子通过,说明电解质溶液为酸性溶液,燃料电池中,通入燃料的电极为负极,负极上失电子发生氧化反应,通入氧化剂的电极为正极,正极上得电子发生还原反应;
(2)原电池反应的实质为氧化还原反应,甲醇被氧化生成二氧化碳和水;
(3)根据甲醇和转移电子之间的关系式计算.
解答 解:(1)该原电池中质子交换膜只允许质子和水分子通过,说明电解质溶液为酸性溶液,燃料电池中,通入燃料的电极为负极,负极上失电子发生氧化反应,电解方程式为CH3OH+H2O-6e-═CO2+6H+,通入氧化剂的电极为正极,正极上得电子发生还原反应,电极方程式为O2+4H++4e-═2H2O,
故答案为:负;CH3OH+H2O-6e-═CO2+6H+;还原;O2+4H++4e-═2H2O;
(2)原电池反应的实质为氧化还原反应,甲醇被氧化生成二氧化碳和水,电池总反应为2CH3OH+3O2=2CO2+4H2O,
故答案为:2CH3OH+3O2=2CO2+4H2O;
(3)由电极方程式CH3OH+H2O-6e-═CO2+6H+可知,如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有$\frac{1}{3}$mol.
故答案为:$\frac{1}{3}$.
点评 本题考查了燃料电池,根据离子交换膜通过的微粒确定电解质溶液的酸碱性,再结合正负极上发生的反应来分析解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.在常温下,把一个盛有一定量甲烷和氯气的密闭玻璃容器放在光亮的地方,两种气体发生反应,下列叙述中不正确的是( )
| A. | 容器内原子总数不变 | B. | 容器内压强不变 | ||
| C. | 容器内分子总数不变 | D. | 发生的反应属于取代反应 |
19.50g碳在空气中燃烧,得到等体积的CO和CO2,已知:C(s)+$\frac{1}{2}{O}_{2}$(g)═CO(g)△H=-110.35kJ•mol-1,CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-282.57kJ•mol-1.损失的能量与实际放出的能量之比大约是( )
| A. | 283:503 | B. | 55:141 | C. | 141:196 | D. | 1:1 |
6.下列化合物的核磁共振氢谱中出现一组峰的是( )
| A. | 2,2,3,3一四甲基丁烷 | B. | 2,3,4一三甲基戊烷 | ||
| C. | 3,4一二甲基己烷 | D. | 2,5一二甲基己烷 |
3.根据如表有机物的排列规律可判断,物质X的同分异构体中能与金属钠反应的(不考虑立体异构)共有( )
| 1 | 2 | 3 | 4 | 5 | 6 | … |
| CH4O | C2H6O | C3H8O | x | C5H12O | C6H14O | … |
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
4.如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )

| A. | 原子半径:Z>Y>X | |
| B. | WX3和水反应形成的化合物是离子化合物 | |
| C. | R的单质可以从W的气态氢化物的水溶液中置换出W的单质 | |
| D. | Z的最高价氧化物对应的水化物既能溶解于盐酸,又能溶解于氨水 |
 ,其中含有的化学键类型为离子键、共价键.
,其中含有的化学键类型为离子键、共价键.