题目内容
6.下列化合物的核磁共振氢谱中出现一组峰的是( )| A. | 2,2,3,3一四甲基丁烷 | B. | 2,3,4一三甲基戊烷 | ||
| C. | 3,4一二甲基己烷 | D. | 2,5一二甲基己烷 |
分析 根据化合物的核磁共振氢谱中出现几组峰,说明有机物中含有几种类型的氢原子,根据等效氢的判断方法来回答.
解答 解:A.2,2,3,3-四甲基丁烷中有1种H原子,核磁共振氢谱中有1组吸收峰,故A正确;
B.2,3,4-三甲基戊烷中有4种H原子,核磁共振氢谱中有4组吸收峰,故B错误;
C.3,4-二甲基己烷中有4种H原子,核磁共振氢谱中有4组吸收峰,故C错误;
D.2,5-二甲基己烷中有3种H原子,核磁共振氢谱中有3组吸收峰,故D错误;
故选A.
点评 本题考查核磁共振氢谱,难度不大,注意利用等效氢原子知识判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列说法正确的是( )
| A. | 原子最外层电子数等于或大于3的元素一定是主族元素 | |
| B. | 原子最外层只有1个电子的元素一定是第IA族元素 | |
| C. | 最外层电子数比次外层电子数多的元素一定位于第二周期 | |
| D. | 某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期 |
1.下列有关同分异构体的叙述正确的是( )
| A. | CH3CH2CH=CHCH2CH3不存在顺反异构体 | |
| B. | 分子式为C5H10O2的羧酸有8种 | |
| C. | 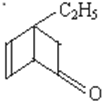 的属于芳香族化合物的同分异构体中不与金属钠反应的有5种 的属于芳香族化合物的同分异构体中不与金属钠反应的有5种 | |
| D. | 棱晶烷  为正三棱柱形,它的二氯代物有5种 为正三棱柱形,它的二氯代物有5种 |
11.固体粉末甲由FeSO4、Fe2(SO4)3、CuSO4、CaCO3、SiO2、NaCl中的若干种组成,取一定量的固体甲进行如下实验:

固体1质量为11g,沉淀1质量为23.3g,沉淀2质量为6g,红褐色固体质量为8g.则下列说法正确的是( )

固体1质量为11g,沉淀1质量为23.3g,沉淀2质量为6g,红褐色固体质量为8g.则下列说法正确的是( )
| A. | 溶液1加入KSCN溶液一定呈红色 | |
| B. | 取少量溶液2加入酸化的硝酸银溶液,生成白色沉淀,则甲中一定有NaCl | |
| C. | 固体1与稀盐酸反应时还生成了标准状况下气体1.12L | |
| D. | 沉淀2不溶于任何酸溶液 |
16.X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是Z元素形成的单质是空气的主要成分之一.已知:甲+乙═丁+己,甲+丙═戊+己; 0.1mol•L-1丁溶液的pH为13(25℃).下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第三周期第ⅣA族 | |
| C. | 1 mol甲与足量的乙完全反应共转移了1 mol电子 | |
| D. | 1.0 L 0.1 mol•L-1戊溶液中阴离子总的物质的量小于0.1 mol |
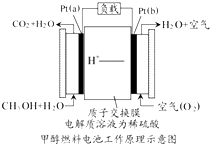 科学家预言,燃料电池将是21世纪获得电能的重要途径,近几年开发甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过,其工作原理的示意图如下:
科学家预言,燃料电池将是21世纪获得电能的重要途径,近几年开发甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过,其工作原理的示意图如下: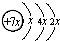 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题: .
.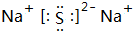 ;W2X2的结构式H-O-O-H.
;W2X2的结构式H-O-O-H.