题目内容
4.如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
| A. | 原子半径:Z>Y>X | |
| B. | WX3和水反应形成的化合物是离子化合物 | |
| C. | R的单质可以从W的气态氢化物的水溶液中置换出W的单质 | |
| D. | Z的最高价氧化物对应的水化物既能溶解于盐酸,又能溶解于氨水 |
分析 短周期元素中,X、W都有最低价-2,处于ⅥA,且W有最高价+6,故X为O、W为S;Y只有+1价,没有负化合价,原子序数大于O,故Y为Na;Z只有+3价,没有负化合价,结合原子序数可知Z为Al;R有+7、-1价,则R为Cl元素,结合元素化合物性质解答.
解答 解:短周期元素中,X、W都有最低价-2,处于ⅥA,且W有最高价+6,故X为O、W为S;Y只有+1价,没有负化合价,原子序数大于O,故Y为Na;Z只有+3价,没有负化合价,结合原子序数可知Z为Al;R有+7、-1价,则R为Cl元素.
A.X为O,Y为Na,Z为Al,同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径应Na>Al>O,故A错误;
B.SO3和水反应形成的化合物是H2SO4,属于共价化合物,故B错误;
C.氯气能与H2S反应生成S与HCl,故C正确;
D.Z的最高价氧化物对应的水化物为氢氧化铝,能溶解于盐酸,不能溶解于氨水,故D错误.
故选C.
点评 本题考查结构性质与位置关系、元素周期律等,难度不大,根据化合价推断元素是解题的关键,侧重对基础知识的巩固.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
12.下列选项不能表示离子反应方程式为H++OH-=H2O的是( )
| A. | NaOH+HCl→NaCl+H2O | B. | 2NaOH+H2SO4→Na2SO4+2H2O | ||
| C. | Ba(OH)2+H2SO4→BaSO4↓+2H2O | D. | Ba(OH)2+2HCl→BaCl2+2H2O |
9.若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物:(1)CH3Cl,(2)CH2Cl2,(3)CHCl3,(4)CCl4,其中正确的是( )
| A. | 只有(1) | B. | 只有(3) | C. | (1)(2)(3)的混合物 | D. | (1)(2)(3)(4)的混合物 |
16.X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是Z元素形成的单质是空气的主要成分之一.已知:甲+乙═丁+己,甲+丙═戊+己; 0.1mol•L-1丁溶液的pH为13(25℃).下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第三周期第ⅣA族 | |
| C. | 1 mol甲与足量的乙完全反应共转移了1 mol电子 | |
| D. | 1.0 L 0.1 mol•L-1戊溶液中阴离子总的物质的量小于0.1 mol |
17.下列说法正确的是( )
| A. | 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 | |
| B. | 一般情况下,一元弱酸HA的Ka 越大,表明该酸的酸性越弱 | |
| C. | 水的离子积只与温度有关,向水中加入酸、碱或盐一定会影响水的电离平衡 | |
| D. | 硅是应用广泛的半导体材料,常温下只与氟气、氢氟酸反应,不和任何其它物质反应 |
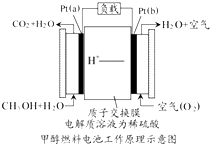 科学家预言,燃料电池将是21世纪获得电能的重要途径,近几年开发甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过,其工作原理的示意图如下:
科学家预言,燃料电池将是21世纪获得电能的重要途径,近几年开发甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过,其工作原理的示意图如下: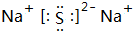 ;W2X2的结构式H-O-O-H.
;W2X2的结构式H-O-O-H.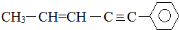 分子结构中在同一平面上的碳原子数最多为11个.
分子结构中在同一平面上的碳原子数最多为11个. I、已知咖啡酸的结构如图所示.
I、已知咖啡酸的结构如图所示. ,A 的同分异构体中只有一种类型的氢原子的结构简式为C(CH3)2═C(CH3)2.
,A 的同分异构体中只有一种类型的氢原子的结构简式为C(CH3)2═C(CH3)2.
 ,①的反应类型为加成反应,一定条件下,1,3-丁二烯反应生成的高分子结构简式为-[CH2-CH=CH-CH2]-n.
,①的反应类型为加成反应,一定条件下,1,3-丁二烯反应生成的高分子结构简式为-[CH2-CH=CH-CH2]-n.