题目内容
某温度下重水(D2O)的离子积常数为1.6×10-15,用定义pH一样来规定pD=-lg{c(D+)},则该温度下,下列叙述正确的是( )
| A、纯净的重水(D2O)中,pD=7 |
| B、1 L溶解有0.01 mol DCl的重水溶液,其pD=12.0 |
| C、纯净的重水中,c(D+)=c(OD-) |
| D、1 L溶解有0.01 mol NaOD的重水溶液,其pD=12.0 |
考点:pH的简单计算,水的电离
专题:
分析:A.根据pD=-lg[D+]计算;
B.根据pD=-lg[D+]计算;
C.纯水显中性;
D.重水(D2O)的离子积常数为1.6×10-15.
B.根据pD=-lg[D+]计算;
C.纯水显中性;
D.重水(D2O)的离子积常数为1.6×10-15.
解答:
解:A.c(D+)=
mol/L=4×10-8mol/L,所以pD>7,故A错误;
B.c(DC1)=
=0.01mol/L,则c(D+)=0.01mol/L,所以pD=2,故B错误;
C.纯水显中性,故c(D+)=c(OD-),故C正确;
D、c(NaOD)=
=0.01mol/L,则c(D+)=
mol/L=1.6×10-13mol/L,则PD>12,则D错误.
故选C.
| 1.6×10-15 |
B.c(DC1)=
| 0.01mol |
| 1L |
C.纯水显中性,故c(D+)=c(OD-),故C正确;
D、c(NaOD)=
| 0.01mol |
| 1L |
| 1.6×10-15 |
| 0.01 |
故选C.
点评:本题考查pH的简单计算,根据溶液的浓度结合离子积常数来解答即可,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案
相关题目
下列叙述正确的是( )
| A、Na2O与Na2O2都能与水反应生成碱,它们都是碱性氧化物 |
| B、Na2CO3溶液和NaHCO3溶液都能与CaCl2溶液反应得到白色沉淀 |
| C、钠在常温下不容易被氧化 |
| D、Na2O2可作供氧剂,而Na2O不行 |
工业上,用辉铜矿(Cu2S)炼铜的方法之一是:①将矿石在高温下鼓入空气煅烧,生成两种氧化物;②将煅烧过的矿石加上比它质量约少一半的未经煅烧过的矿石,混合后隔绝空再进行高温煅烧,结果得到铜和一种有刺激性气味的气体.下列对反应①和②的推断不正确的是( )
| A、反应①和②的氧化产物都是S02 |
| B、反应①的氧化产物与还原产物物质的量之比为1:1 |
| C、等物质的量的硫化亚铜在反应①和②中完全反应,转移的电子数相等 |
| D、反应②中,硫化亚铜既是氧化剂又是还原剂 |
短周期元素X、Y、Z原子序数依次增大,X原子的核外电子数与Y原子的最外层电子数相等,Y原子的最外层电子数是内层电子数的3倍,Z的原子半径大于Y,Z与R能形成离子化合物RZ2,且两种离子具有相同的电子层结构.下列判断正确的是( )
| A、X与Y形成的分子中既含有极性共价键又含有非极性共价键 |
| B、X的气态氢化物比Y的气态氢化物稳定 |
| C、X与R、Y与R均能形成阴阳离子数目之比为1:1的化合物 |
| D、R、X、Y三种元素可形成化学式为RXY3、R(X2Y4)2的两种盐 |
下列表达方式正确的是( )
A、碳-12原子
| ||
B、羟基电子式 | ||
C、硫离子结构示意图 | ||
D、CH4S的结构式 |
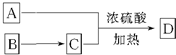 所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式
所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式