题目内容
在乙醇发生的各种反应中,断键方式不正确的是( )
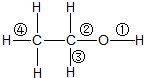

| A、与金属钠反应时,键①断裂 |
| B、与醋酸、浓硫酸共热时,键②断裂 |
| C、与HCl反应生成氯乙烷时,键②断裂 |
| D、与浓硫酸共热至170℃时,键②和④断裂 |
考点:乙醇的化学性质
专题:有机反应
分析:A、乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键;
B、乙醇与酸发生酯化反应,断开的羟基上的氢氧键;
C、与HCl反应生成氯乙烷时,-OH被-Cl取代,C-O键断裂;
D、乙醇和浓硫酸共热到170℃时发生消去反应,断裂碳氧键、与羟基所连的碳的相邻的碳上的碳氢键.
B、乙醇与酸发生酯化反应,断开的羟基上的氢氧键;
C、与HCl反应生成氯乙烷时,-OH被-Cl取代,C-O键断裂;
D、乙醇和浓硫酸共热到170℃时发生消去反应,断裂碳氧键、与羟基所连的碳的相邻的碳上的碳氢键.
解答:
解:A、与金属钠反应时,生成乙醇钠和氢气,O-H键断裂,即键①断裂,故A正确;
B、与醋酸、浓硫酸共热时,发生酯化反应,醇脱H,O-H键断裂,即键①断裂,故B错误;
C、与HCl反应生成氯乙烷时,-OH被-Cl取代,C-O键断裂,即键②断裂,故C正确;
D、与浓硫酸共热至170℃时,发生消去反应生成乙烯和水,C-O、C-H键断裂,即键②和④断裂,故D正确;
故选B.
B、与醋酸、浓硫酸共热时,发生酯化反应,醇脱H,O-H键断裂,即键①断裂,故B错误;
C、与HCl反应生成氯乙烷时,-OH被-Cl取代,C-O键断裂,即键②断裂,故C正确;
D、与浓硫酸共热至170℃时,发生消去反应生成乙烯和水,C-O、C-H键断裂,即键②和④断裂,故D正确;
故选B.
点评:本题考查有机物的结构与性质,把握官能团与性质的关系为解答的关键,侧重醇性质的考查,注意发生的反应及化学键的断裂位置,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验装置图所示的实验操作,不能达到相应的实验目的是( )
A、 检查装置气密性 |
B、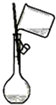 向容量瓶中转移液体 |
C、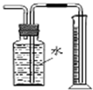 测量Cu与浓硝酸产生气体体积 |
D、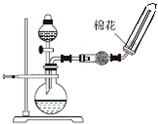 实验室制取并收集NH3 |
以下分离混合物的操作中,不正确的是( )
A、蒸发时,蒸发皿内所盛液体不超过蒸发皿容积的
| ||
| B、蒸发结晶时,不能直接蒸干液体,最后少量液体用余热蒸干 | ||
| C、用四氯化碳萃取碘水中的碘,分液时四氯化碳碘溶液从上口倒出 | ||
| D、蒸馏时,要在烧瓶中加入几粒碎瓷片 |
关于实验室中的下列叙述,正确的是( )
| A、金属钠着火燃烧时,用泡沫灭火器灭火 |
| B、硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中 |
| C、在新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液最终呈红色 |
| D、向Ba(OH)2溶液中慢慢滴加稀硫酸至过量,溶液的导电性变化是弱→强→弱 |
下列物质属于塑料的是( )
| A、玻璃 | B、锦纶 | C、蔗糖 | D、聚乙烯 |
某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀.该有机样品是( )
| A、乙二醇(C2H6O2) |
| B、乙醇 |
| C、乙醛 |
| D、甲烷和丙烷(C3H8)的混合物 |
将几滴KSCN(SCN-是“类卤离子”,与氯离子性质相似)溶液加入酸性的含有Fe3+的溶液中,溶液变成血红色.将该红色溶液分为两份,①一份中加入适量KMnO4溶液,红色褪去;②向另一份中通入SO2,红色也褪去.下列说法不正确的是( )
| A、①红色褪去的原因可能是KMnO4将SCN-氧化,使[Fe(SCN)]2+消失 |
| B、[Fe(SCN)]2+中Fe3+与SCN-以配位键结合 |
| C、②红色褪去的原因是SO2具有还原性 |
| D、SCN-在适当条件下可被还原为(SCN)2 |
下列说法正确的是( )
| A、CO2的水溶液能导电,所以CO2是电解质 |
| B、氧化剂在反应中得到的电子越多,氧化能力越强 |
| C、用加热法可分离I2和NH4HCO3两种固体 |
| D、Cl2的氧化性比I2强,而I-的还原性却比Cl-强 |
 分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )
分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )