��Ŀ����
��298Kʱ��NaCl ��ˮ�е��ܽ��Ϊ
ˮ���罫1molNaCl�ܽ���1Lˮ�У����ܽ��������ϵ�ġ�H-T��S������α仯��������
| 26g |
| 100g |
| A����H-T��S��0��S��0 |
| B����H-T��S��0��S��0 |
| C����H-T��S��0��S��0 |
| D����H-T��S��0��S��0 |
���㣺�ʱ���ر�
ר�⣺��ѧ��Ӧ�е������仯
����������NaCl �ܽ���ˮ�Ĺ������Է����̣����ԡ�H-T��S��0��NaCl �Ӿ�������Һ�����Ҷ��������ԡ�S��0��
���
�⣺����NaCl�ܽ���ˮ�Ĺ������Է����̣����ԡ�H-T��S��0��
NaCl�Ӿ�������Һ�����Ҷ����������ӣ����ԡ�S��0��
��ѡB��
NaCl�Ӿ�������Һ�����Ҷ����������ӣ����ԡ�S��0��
��ѡB��
���������⿼�����Է����̵��жϣ�������״̬���ر�Ĺ�ϵ�����ܽ���أ��ѶȲ���ע����ݽ̲����й�֪ʶ�������ɣ�

��ϰ��ϵ�д�
�����Ŀ
Fe 2��SO4��3�е���Ԫ����������Ϊ2a%������Ԫ�ص���������Ϊ��������
| A��1-a% |
| B��1-2 a% |
| C��1-3 a% |
| D��3 a% |
��NA��ʾ�����ӵ�����������������ȷ���ǣ�������
| A����������N2��CO������������ΪNA |
| B�����³�ѹ�£�1.06 g Na2CO3���е�Na+������Ϊ0.2NA |
| C��2.4 g����þ��Ϊþ����ʱʧȥ�ĵ�����Ϊ0.1NA |
| D�����³�ѹ��48gO2��48gO3���е���ԭ������Ϊ3NA |
�������ʵ�ˮ��Һ�ܵ��磬�����ڷǵ���ʵ��ǣ�������
| A��Na2O |
| B��Cl2 |
| C��NH4HCO3 |
| D��CO2 |
�������������˵����ȷ���ǣ�������
| A������Ԫ�صĻ�������һ������� |
B����Ϊ���Ӽ���������Ե�ʣ�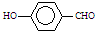 �� ��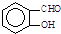 �۷е�� �۷е�� |
| C����������ȷ��»���ǿ������H2O���ӱ�H2S�����ȶ� |
| D������ȼ����--����ˮ������磺8CH4?46H2O����CH4��H2O֮�������� |
 ij�о���ѧϰС���������²�����̽��NH3�Ļ�ԭ�ԣ�����ʵ��װ������ͼ������1��NH3��ǿ��ԭ�����ܽ�ijЩ���������ﻹԭΪ�������ʻ�ͼ�̬��������磺2NH3+3CuO
ij�о���ѧϰС���������²�����̽��NH3�Ļ�ԭ�ԣ�����ʵ��װ������ͼ������1��NH3��ǿ��ԭ�����ܽ�ijЩ���������ﻹԭΪ�������ʻ�ͼ�̬��������磺2NH3+3CuO