题目内容
14.25℃时,下列各组微粒在指定溶液中一定能大量共存的是( )| A. | 滴加酚酞试液显红色的溶液中:K+、Na+、NO3-、Cl- | |
| B. | c(H+)=1×10-13 mol•L-1的溶液中:Mg2+、Na+、SO42-、NO3- | |
| C. | pH=1的溶液中:Na+、K+、MnO4-、SO2 | |
| D. | 0.1 mol•L-1FeCl3溶液中:Ba2+、Na+、SCN-、Br- |
分析 A.滴加酚酞试液显红色的溶液为碱性溶液,四种离子之间不反应,都不与氢氧根离子反应;
B.c(H+)=1×10-13 mol•L-1的溶液中存在大量氢氧根离子,镁离子与氢氧根离子反应;
C.该溶液为酸性溶液,高锰酸根离子酸性条件下能够氧化二氧化硫;
D.铜离子与硫氰根离子发生反应生成络合物硫氰化铁.
解答 解:A.滴加酚酞试液显红色的溶液中存在大量氢氧根离子,之间不反应,K+、Na+、NO3-、Cl-都不与氢氧根离子反应,在溶液中能够大量共存,故A正确;
B.c(H+)=1×10-13 mol•L-1的溶液为碱性溶液,溶液中存在大量氢氧根离子,Mg2+与氢氧根离子反应生成氢氧化镁沉淀,在溶液中不能大量共存,故B错误;
C.pH=1的溶液为酸性溶液,MnO4-、SO2在酸性溶液中发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.Fe3+和 SCN-之间反应生成硫氰化铁,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
4.雾霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一.消除氮氧化物和硫氧化物有多种方法.可用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)═N2(g)+CO2(g)△H=Q kJ•mol-1.在T1℃时,反应进行到不同时间测得各物质的浓度如下:
0~10min内,CO2的平均反应速率v(CO2)=0.021mol/(L.min),反应进行到30min时,NO 的转化率=60%.
| 时间(min) 浓度(mol•L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
2.中学化学中有很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 强酸可以制弱酸 | 氢硫酸(H2S)无法制取硫酸 |
| B | 反应物浓度越大,反应速度越快 | 常温下,相同的铝片分别加入到浓、稀硫酸中,浓硫酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随着相对分子质量增大而升高 | NH3的沸点低于PH3 |
| D | 溶解 度小的沉淀易向溶解度更小的沉淀转化 | AgCl沉淀中滴定KI溶液,会得到AgI沉淀 |
| A. | A | B. | B | C. | C | D. | D |
19.乙醇和乙酸是生活中重要的两种有机物,下列有关说法正确的是( )
| A. | 都含有不饱和键 | |
| B. | 等质量的两种有机物完全燃烧时,所消耗氧气的质量相等 | |
| C. | 都能发生加成反应、取代反应和氧化反应 | |
| D. | 含有不同的官能团 |
4.能正确表示下列反应的离子方程式是( )
| A. | 氢氧化亚铁溶于稀硝酸中:Fe(OH)2+2H+═Fe2++2H2O | |
| B. | 三氧化二铁溶于氢碘酸:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 铝与氢氧化钠溶液反应:2AI+2OH-═2 AIO2-+H2↑ | |
| D. | 在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
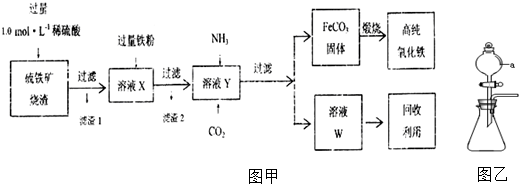
 地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题.文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响.
地下水中硝酸盐造成的氮污染已成为一个世界性的环境问题.文献报道某课题组模拟地下水脱氮过程,利用Fe粉和KNO3溶液反应,探究脱氮原理及相关因素对脱氮速率的影响.
 ;
;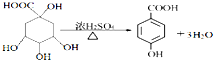 _,反应类型是消去反应;
_,反应类型是消去反应; (其中任一种);(任写一种)
(其中任一种);(任写一种) .
.