题目内容
3.以下为中学化学中常见物质的转化关系图,反应条件及部分反应物和产物未全部注明,已知A、D为常见金属单质,其他均为化合物.且知B为具有磁性的氧化物,I在空气中转化为J的现象是白色沉淀迅速变为灰绿色,最后变为红褐色.而试剂 ①②则为常见的酸、碱溶液.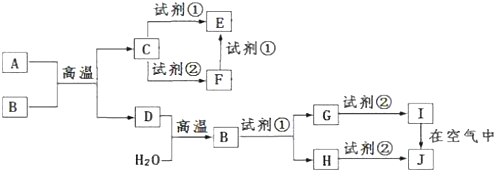
试回答下列问题:
(1)试剂 ①可以是下列物质中的d.
a.NaOH溶液 b.浓氨水 c.稀硝酸 d.稀盐酸
(2)A、C、E、F四种物质中所含的同一种元素是Al.
(3)写出物质B、C的化学式:B:Fe3O4;C:Al2O3.
(4)写出下列反应的方程式:
A→F的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑;
I→J的化学方程式4Fe(OH)2+O2+2H2O=4Fe(OH)3;
试剂②可以由一种淡黄色固体粉末和一种常见液体发生反应而制得,其相应的离子方程式2Na2O2+2H2O=4Na++4OH-+O2↑.
(5)某同学认为J中可能同时含有同一种金属元素的两种阳离子,若要确认其中低价金属阳离子的存在,应选用d(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性高锰酸钾溶液.
分析 A、D是常见的金属单质,且B为具有磁性的氧化物,I在空气中转化为J的现象是白色沉淀迅速变为灰绿色,最后变为红褐色,结合转化关系可知,B为Fe3O4、D为Fe、I为Fe(OH)2、J为Fe(OH)3,试剂①为酸,试剂②为碱,G为亚铁盐,H为铁盐,由①可知C为金属氧化物,且能与酸、碱反应,可推知A为Al、C为Al2O3,C与试剂①得到E,则E为铝盐,C与试剂②得到F,F与试剂①得到E,故F为偏铝酸盐,据此解答.
解答 解:A、D是常见的金属单质,且B为具有磁性的氧化物,I在空气中转化为J的现象是白色沉淀迅速变为灰绿色,最后变为红褐色,结合转化关系可知,B为Fe3O4、D为Fe、I为Fe(OH)2、J为Fe(OH)3,试剂①为酸,试剂②为碱,G为亚铁盐,H为铁盐,由①可知C为金属氧化物,且能与酸、碱反应,可推知A为Al、C为Al2O3,C与试剂①得到E,则E为铝盐,C与试剂②得到F,F与试剂①得到E,故F为偏铝酸盐.
(1)试剂 ①为酸,且能与氧化铝反应,与四氧化三铁反应得到亚铁盐、铁盐,应是非氧化性酸,而硝酸具有强氧化性,故可以为稀盐酸,故答案为:d;
(2)A、C、E、F四种物质中所含的同一种元素是:Al元素,故答案为:Al;
(3)由上述分析可知,B为Fe3O4,C为Al2O3,故答案为:Fe3O4;Al2O3;
(4)A→F的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑;
I→J的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
试剂②可以由一种淡黄色固体粉末和一种常见液体发生反应而制得,应是过氧化钠与水反应生成氢氧化钠与氧气,其相应的离子方程式:2Na2O2+2H2O=4Na++4OH-+O2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;4Fe(OH)2+O2+2H2O=4Fe(OH)3;2Na2O2+2H2O=4Na++4OH-+O2↑;
(5)某同学认为J中可能同时含有同一种金属元素的两种阳离子,要确认其中低价亚铁离子离子的存在,由于亚铁离子具有还原性,可以使酸性高锰酸钾溶液,故选:d.
点评 本题考查无机物推断,涉及Fe、Al元素单质化合物性质,“B的性质、I转化为J的现象”是推断突破口,侧重对化学用语的考查,难度不大,注意基础知识的掌握.

| A. | 第2周期第ⅣA族 | B. | 第3周期第ⅣA族 | C. | 第4周期第ⅡA族 | D. | 第3周期第ⅥA族 |
| A. | 滴加酚酞试液显红色的溶液中:K+、Na+、NO3-、Cl- | |
| B. | c(H+)=1×10-13 mol•L-1的溶液中:Mg2+、Na+、SO42-、NO3- | |
| C. | pH=1的溶液中:Na+、K+、MnO4-、SO2 | |
| D. | 0.1 mol•L-1FeCl3溶液中:Ba2+、Na+、SCN-、Br- |
| A. | Cl2溶于水:Cl2+H2O=2H++Cl-+ClO- | |
| B. | NaHCO3溶液中加入HCl:CO32-+2H+=CO2↑+H2O | |
| C. | 少量二氧化碳通入足量的NaOH溶液:CO2+OH-═HCO3- | |
| D. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O |
| A. | 因为碳酸、氨水能够导电,所以液氨、二氧化碳是电解质 | |
| B. | 由同种元素组成的物质一定是纯净物 | |
| C. | 由C(石墨)═C(金刚石);△H=+1.90kJ•mol-1可知,石墨比金刚石稳定 | |
| D. | 在101kPa时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,则表示氢气燃烧的热化学方程式为:2H2(g)+O2 (g)═2H2O(l);△H=-285.8kJ•mol-1 |
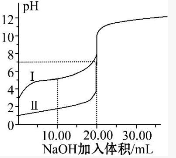 室温下,用0.100mol•L-1NaOH溶液分别滴定20.00mL 0.100mol•L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol•L-1NaOH溶液分别滴定20.00mL 0.100mol•L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )| A. | Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线 | |
| B. | V(NaOH)=10.00 mL时,QUOTE>1 | |
| C. | 当V(NaOH)=20.00 mL时,两种酸溶液的pH均等于7 | |
| D. | V(NaOH)=20.00 mL时,c(Cl-)<c(CH3COO-) |
| A. | 点燃的酒精灯不小心打翻了,应立即用自来水灭火 | |
| B. | 皮肤沾上少量浓硫酸后,可先用大量水冲洗,再涂上稀碳酸氢钠溶液 | |
| C. | 在蒸馏实验中,加热一段时间后,忘了加入沸石,打开瓶塞立即加入沸石 | |
| D. | 冷凝管用作冷凝回流时,为防止有机物蒸汽逸出,可使用橡胶塞塞住顶端出口 |
| A. | ①② | B. | ③④ | C. | ①②③④ | D. | ①②③④⑤ |
 为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如图实验,请回答下列问题:
为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如图实验,请回答下列问题: