题目内容
5.下列物质既属于无机物,又属于碱的是( )| A. | Na2CO3 | B. | CH3OH | C. | Al2O3 | D. | Cu(OH)2 |
分析 大多数无机物中不含碳元素,碱是指电离出的阴离子全部是氢氧根离子的化合物,据此回答判断.
解答 解:A、碳酸钠属于盐,不属于碱,故A错误;
B、甲醇属于有机物,故B错误;
C、氧化铝属于氧化物,不属于碱,故C错误;
D、氢氧化铜属于无机物,电离出的阴离子全部是氢氧根离子,属于碱,故D正确.
故选D.
点评 本题考查学生无机物和碱的概念知识,属于基本知识的考查,注意概念的理解和把握是关键,难度中等.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
15.下列变化过程需要吸收能量的是( )
| A. | 白磷在空气中自燃 | B. | CaO+H2O=Ca(OH)2 | ||
| C. | 酸碱中和反应 | D. | H2→H+H |
16.实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
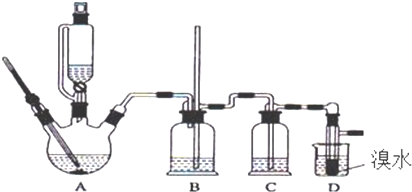
有关数据列表如下:
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
(2)装置B的作用是平衡压强,作安全瓶,防止倒吸.
(3)在装置C中应加入d (填字母).
a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(4)若产物中有少量未反应的Br2,最好用e(填字母)洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是产品熔点低,过度冷却会凝固而堵塞导管口.
(7)判断该制备反应已经结束的最简单方法是D中溴水完全褪色.

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
(1)烧瓶A中发生的主要的反应方程式CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
(2)装置B的作用是平衡压强,作安全瓶,防止倒吸.
(3)在装置C中应加入d (填字母).
a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(4)若产物中有少量未反应的Br2,最好用e(填字母)洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是产品熔点低,过度冷却会凝固而堵塞导管口.
(7)判断该制备反应已经结束的最简单方法是D中溴水完全褪色.
13.下列关于胶体,判断正确的是( )
| A. | 煮沸饱和FeCl3溶液可以制得Fe(OH)3胶体 | |
| B. | 胶体的本质特征是胶粒半径在1~100nm | |
| C. | 丁达尔现象可以用来区别胶体和溶液 | |
| D. | 溶液能通过滤纸孔隙而胶体的分散质不能通过 |
20.氧化还原反应的实质是( )
| A. | 是否有电子转移 | |
| B. | 同一元素的化合价在反应前后是否有变化 | |
| C. | 是否有氧元素参加 | |
| D. | 是否是化合反应或分解反应 |
10.下列反应中,能放出气体,又属于非氧化还原反应的是( )
| A. | 浓盐酸与二氧化锰共热 | B. | 浓硫酸与铜共热 | ||
| C. | 过氧化钠与水反应 | D. | 石灰石与稀盐酸反应 |
17.下列化学仪器能用于加热的是( )
| A. | 容量瓶 | B. | 圆底烧瓶 | C. | 试管 | D. | 烧杯 |
14.在一定温度下,可逆反应A2(g)+B2(g)═2AB(g)达到化学平衡的标志是 ( )
| A. | 容器内气体的总质量不随时间而变化 | |
| B. | 单位时间内有nmolA2生成的同时就有nmolB2生成 | |
| C. | 2 v(A2)正=v(AB)逆 | |
| D. | A2、B2(g)、AB(g)的浓度之比为1:1:2 |
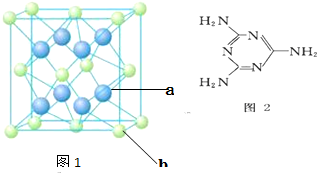 X、Y、Z、M、N、Q P为元素周期表前四周期的7种元素.其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大.P元素的第三电子层处于全充满状态,第四电子层只有一个电子请回答下列问题:
X、Y、Z、M、N、Q P为元素周期表前四周期的7种元素.其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大.P元素的第三电子层处于全充满状态,第四电子层只有一个电子请回答下列问题: ,P元素属于ds区元素.
,P元素属于ds区元素.