题目内容
短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z+与Y2-具有相同的电子层结构,W与Y同主族.下列说法正确的是( )
| A、原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B、Z在周期表中的位置为第3周期、IB族 |
| C、X的最高价氧化物对应水化物的酸性比W的弱 |
| D、W比Y更容易与氢气反应 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期主族元素X、Y、Z、W的原子序数依次增大,Y是地壳中含量最高的元素,则Y是O元素;
W与Y同一主族且属于短周期元素,则W是S元素;
X原子的最外层电子数是其内层电子数的2倍,最外层电子数不超过8个,且X原子序数小于Y,则X是C元素;
Z+与Y2-具有相同的电子层结构,则Z是Na元素,
A.电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
B.主族元素电子层数与其周期数相等、最外层电子数与其族序数相等;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
D.元素的非金属性越强,其气态氢化物越稳定.
W与Y同一主族且属于短周期元素,则W是S元素;
X原子的最外层电子数是其内层电子数的2倍,最外层电子数不超过8个,且X原子序数小于Y,则X是C元素;
Z+与Y2-具有相同的电子层结构,则Z是Na元素,
A.电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
B.主族元素电子层数与其周期数相等、最外层电子数与其族序数相等;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
D.元素的非金属性越强,其气态氢化物越稳定.
解答:
解:短周期主族元素X、Y、Z、W的原子序数依次增大,Y是地壳中含量最高的元素,则Y是O元素;
W与Y同一主族且属于短周期元素,则W是S元素;
X原子的最外层电子数是其内层电子数的2倍,最外层电子数不超过8个,且X原子序数小于Y,则X是C元素;
Z+与Y2-具有相同的电子层结构,则Z是Na元素,
A.电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径r(Z)>r(W)>r(X)>r(Y),故A错误;
B.主族元素电子层数与其周期数相等、最外层电子数与其族序数相等,Z原子核外有3个电子层、最外层有1个电子,所以位于第三周期第IA族,故B错误;
C.非金属性X<W,所以X的最高价氧化物对应水化物的酸性比W的弱,故C正确;
D.非金属性Y>W,所以Y比W容易与氢气反应,故D错误;
故选C.
W与Y同一主族且属于短周期元素,则W是S元素;
X原子的最外层电子数是其内层电子数的2倍,最外层电子数不超过8个,且X原子序数小于Y,则X是C元素;
Z+与Y2-具有相同的电子层结构,则Z是Na元素,
A.电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径r(Z)>r(W)>r(X)>r(Y),故A错误;
B.主族元素电子层数与其周期数相等、最外层电子数与其族序数相等,Z原子核外有3个电子层、最外层有1个电子,所以位于第三周期第IA族,故B错误;
C.非金属性X<W,所以X的最高价氧化物对应水化物的酸性比W的弱,故C正确;
D.非金属性Y>W,所以Y比W容易与氢气反应,故D错误;
故选C.
点评:本题考查原子结构和元素周期律的关系,侧重考查元素周期律的运用,明确元素原子半径比较方法、非金属性与其最高价氧化物的水化物酸性及与氢气化合难易程度即可解答,题目难度不大.

练习册系列答案
相关题目
将氯气溶于草木灰的浸出液所得溶液比氯水的漂白能力强而且无逸出氯气的有害作用.请你根据所学知识判断下列说法错误的是( )
| A、碳酸的酸性弱于盐酸,但强于次氯酸 |
| B、氯气通入草木灰的溶液中发生反应2K2CO3+Cl2+H2O═2KHCO3+KCl+KClO |
| C、氯气通入草木灰的溶液中发生反应K2CO3+Cl2+H2O═KHCO3+KCl+HClO |
| D、草木灰溶液本身不具有漂白作用,但具有去污作用 |
从溴乙烷制取1,2-二溴乙烷,下列转化方案中最好的是( )
A、CH3CH2Br
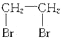 | |||||||
B、CH3CH2Br
| |||||||
C、CH3CH2Br
| |||||||
D、CH2=CH2
|
有关化学用语表达正确的是( )
A、聚苯乙烯的结构简式: | ||||
B、S2-的结构示意图: | ||||
C、
| ||||
D、过氧化氢电子式: |
有关物质用途,用离子方程式解释不正确的是( )
| A、氢氟酸刻蚀玻璃:SiO2+4HF=SiF4↑+2H2O |
| B、明矾用于净水:Al3++3H2O=Al(OH)3+3H+ |
| C、纯碱去除油污:CO32-+H2O?HCO3-+OH- |
| D、氯气制备“84”消毒液:Cl2+2OH-=Cl-+ClO-+H2O |

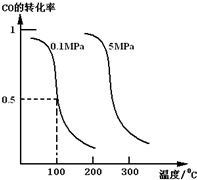 研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)?CH3OH(g).
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题.在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)?CH3OH(g).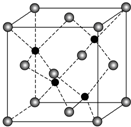 X、Y、Z、R、Q为前四周期元素,且原子序数依次增大,其中Y原子核外2p能级上有1个电子,R原子L层上有2对成对电子,X与Z可形成共价化合物ZX3,Q原子在第四周期中未成对电子数最多.请回答下列问题:
X、Y、Z、R、Q为前四周期元素,且原子序数依次增大,其中Y原子核外2p能级上有1个电子,R原子L层上有2对成对电子,X与Z可形成共价化合物ZX3,Q原子在第四周期中未成对电子数最多.请回答下列问题: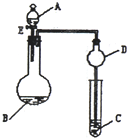 用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题: