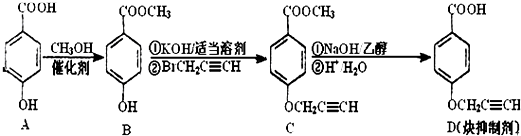
题目内容
从溴乙烷制取1,2-二溴乙烷,下列转化方案中最好的是( )
A、CH3CH2Br
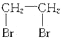 | |||||||
B、CH3CH2Br
| |||||||
C、CH3CH2Br
| |||||||
D、CH2=CH2
|
考点:溴乙烷的制取
专题:有机物的化学性质及推断
分析:在有机物的制备反应中,应选择的合成路线是步骤尽量少,合成产率尽量高,据此解答即可.
解答:
解:A、溴乙烷与溴化氢溶液不能反应,故A错误;
B、取代在有机物的制备反应中,取代位置不一,可能生成1,1-二溴乙烷,故B错误;
C、最后一步中,产物不唯一,故C错误;
D、应选择的合成路线是步骤尽量少,合成产率尽量高.对此题而言,选择加成反应要比取代反应好得多,而使用加成反应,必须先发生消去反应生成不饱和烃,显然D的步骤少,且产物唯一,故D正确,
故选D.?
B、取代在有机物的制备反应中,取代位置不一,可能生成1,1-二溴乙烷,故B错误;
C、最后一步中,产物不唯一,故C错误;
D、应选择的合成路线是步骤尽量少,合成产率尽量高.对此题而言,选择加成反应要比取代反应好得多,而使用加成反应,必须先发生消去反应生成不饱和烃,显然D的步骤少,且产物唯一,故D正确,
故选D.?
点评:本题主要考查的是有机物的制备方案的设计,有机物的制备应尽量步骤少、产率高,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ | ||
| B、由水电离的C(H+)=1×10-14mol?L-1的溶液中:Ca2+、K+、Cl-、HCO3- | ||
C、
| ||
| D、c(Fe3+)=0.1mol?L-1的溶液中:K+、SO42-、CO32-、Cl- |
恒温条件下,将NO2装入带活塞的密闭容器中,当反应2NO2(g)?N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是( )
| A、若体积减小一半,则压强为原来的两倍 |
| B、平衡向右移动,混合气体颜色一定会变浅 |
| C、若体积减小一半,压强增大,但小于原来的两倍 |
| D、平衡向右移动,混合气体密度减小 |
短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z+与Y2-具有相同的电子层结构,W与Y同主族.下列说法正确的是( )
| A、原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B、Z在周期表中的位置为第3周期、IB族 |
| C、X的最高价氧化物对应水化物的酸性比W的弱 |
| D、W比Y更容易与氢气反应 |
下列关于氯的说法错误的是( )
| A、氯水、液氯中均含有Cl2分子,故两者均为黄绿色 | ||||
B、
| ||||
| C、Cl2可以使湿润的有色布条褪色,是因为Cl2有漂白性 | ||||
| D、氯水中分子由多到少的顺序是:H2O>Cl2>HClO |