题目内容
2.NA表示阿佛加德罗常数,下列说法正确的是( )| A. | 1mol乙烷中含有6NA个共价键 | |
| B. | 1mol乙醇与足量乙酸在浓硫酸催化下反应可生成1mol乙酸乙酯 | |
| C. | 1mol某饱和醇(可看成是烷烃中的氢被羟基取代的产物)与足量的金属钠反应产生1molH2,说明其一个分子中含有两个羟基 | |
| D. | 1mol乙烯发生加成反应其断裂2mol共价键 |
分析 A.根据乙烷分子的物质的量及结构计算出含有的共价键数目;
B.羧酸与醇的酯化反应是可逆反应;
C.依据1mol-OH和钠反应生成0.5molH2;
D.1mol乙烯分子中含1mol碳碳双键发生加成反应断裂1mol共价键;
解答 解:A.1mol乙烷分子中含有1mol碳碳共价键和6mol碳氢共价键,总共含有7mol共价键,1 mol乙烷分子中共价键总数为7NA,故A错误;
B.乙酸与乙醇反应生成乙酸乙酯,属于可逆反应,反应物不能完全转化,反应可生成乙酸乙酯物质的量小于1mol,故B错误;
C.1mol-OH和钠反应生成0.5molH2,1mol某饱和醇(可看成是烷烃中的氢被羟基取代的产物)与足量的金属钠反应产生1molH2,2-OH~2Na~H2,说明其一个分子中含有两个羟基,故C正确;
D.1mol-OH和钠反应生成0.5molH2,1mol乙烯分子中含1mol碳碳双键发生加成反应断裂1mol共价键,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是有机物结构、有机物反应实质理解应用,掌握有机物的据此知识是解题关键,题目难度中等.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
12.工业上制备纯净的氯化锌时,将含杂质的氯化锌溶于过量盐酸中,为了除去杂质需调节溶液的pH到4,应加入的试剂是( )
| A. | NaOH | B. | NH3•H2O | C. | ZnO | D. | ZnCl2 |
13.2014年5月17日,南京的一家公司4名工作人员在放射源操作和保管过程中违反相关规定,导致放射源${\;}_{77}^{192}$Ir丢失的事件,${\;}_{77}^{192}$Ir是由${\;}_{77}^{193}$Ir经过中子辐射后获得,下列有关说法正确的是( )
| A. | ${\;}_{77}^{192}$Ir和${\;}_{77}^{193}$Ir是两种核素 | |
| B. | ${\;}_{77}^{192}$Ir和${\;}_{77}^{193}$Ir是两种元素 | |
| C. | Ir是主族元素 | |
| D. | 由${\;}_{77}^{193}$Ir经过中子辐射后获得${\;}_{77}^{192}$Ir是化学变化 |
10.下列液体中,不会出现丁达尔效应的分散系是( )
①鸡蛋白溶液 ②水 ③淀粉溶液 ④硫酸钠溶液 ⑤Fe(OH)3胶体 ⑥泥浆水.
①鸡蛋白溶液 ②水 ③淀粉溶液 ④硫酸钠溶液 ⑤Fe(OH)3胶体 ⑥泥浆水.
| A. | ②④ | B. | ③④⑥ | C. | ②④⑥ | D. | ④⑥ |
17.实验室中进行粗盐提纯时,下列试剂添加过程中不符合绿色化学的是( )
| A. | BaCl2→Na2CO3 | B. | Na2CO3→HCl | C. | Na2CO3→Ca(OH)2 | D. | 水→BaCl2 |
11.下列说法中不正确的是( )
| A. | 第一电离能由大到小的顺序为N>O>C | |
| B. | 由于C22-和O22+为等电子体,所以可以判断O22+的电子式为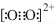 | |
| C. | NO3-中N采用sp2杂化,故NO3-的空间构型为三角锥形 | |
| D. | 液态HF通常也可以写成(HF)n的形式,是因为液态HF分子间存在氢键 |
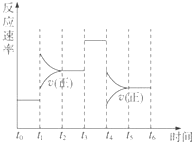 在体积固定的密闭体系中发生下列反应:
在体积固定的密闭体系中发生下列反应: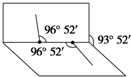 解答下列问题,本题共两个小题.
解答下列问题,本题共两个小题.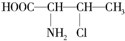 ,一个该有机物分子中含有2个手性碳原子.其中一对对映异构体用简单的投影式表示为:
,一个该有机物分子中含有2个手性碳原子.其中一对对映异构体用简单的投影式表示为: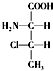 和
和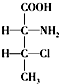 ,则另一对对映异构体的简单投影式为:
,则另一对对映异构体的简单投影式为: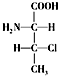 和
和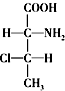 .②②
.②②