题目内容
7. 在体积固定的密闭体系中发生下列反应:
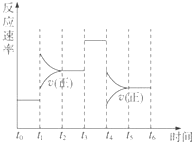
在体积固定的密闭体系中发生下列反应:A(g)+3B(g)?2C(g)△H<0,图是某一时间段中反应速率与反应进程的曲线关系,完成下列问题:
(1)t1、t3、t4时刻体系中所改变的条件可能是C、E、B(选填下列序号字母).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(2)C体积分数最高的时间段是t0~t1.(填“tx-ty”)
分析 (1)根据温度、催化剂以及压强对反应速率的影响分析,注意各时间段正逆反应速率的变化;
(2)t1~t2,t4~t5,反应向逆反应方向移动,随着反应的进行,生成的C逐渐减小,C的体积分数逐渐减小.
解答 解:(1)t1时,正逆反应速率都增大,且逆反应速率大于正反应速率,反应向逆反应方向移动,则应为升高温度的变化,故选C;
t3时,正逆反应速率都增大,正逆反应速率相等,平衡不移动,应为加入催化剂的变化,故选E;
t4时,正逆反应速率都减小,且逆反应速率大于正反应速率,平衡向逆反应方向移动,由方程式计量数关系可知,应为减小压强的变化,故选B,
故答案为:C;E;B;
(2)t1~t2,t4~t5,反应向逆反应方向移动,随着反应的进行,生成的C逐渐减小,C的体积分数逐渐减小,故C体积分数最高的时间段是t0~t1,
故答案为:t0~t1.
点评 本题考查化学反应速率的变化曲线,题目难度中等,注意化学方程式的特点,判断温度、压强对反应平衡移动的影响,结合外界条件对反应速率的影响分析,试题培养了学生的分析、理解能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17. X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A. | 四种元素的单质中,Z的熔沸点最低 | |
| B. | 最高价氧化物对应水化物的酸性W比Z弱 | |
| C. | Y的气态氢化物的稳定性较Z的弱 | |
| D. | 离子半径:Z>W>X>Y |
18.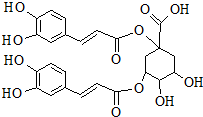 洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是( )
洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是( )
 洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是( )
洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是( )| A. | 1mol洋蓟素最多可与6molBr2反应 | |
| B. | 1mol洋蓟素最多可与7molNa2CO3反应 | |
| C. | 一定条件下能发生酯化反应和消去反应 | |
| D. | 1mol洋蓟素最多可与9molNaOH反应 |
2.NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 1mol乙烷中含有6NA个共价键 | |
| B. | 1mol乙醇与足量乙酸在浓硫酸催化下反应可生成1mol乙酸乙酯 | |
| C. | 1mol某饱和醇(可看成是烷烃中的氢被羟基取代的产物)与足量的金属钠反应产生1molH2,说明其一个分子中含有两个羟基 | |
| D. | 1mol乙烯发生加成反应其断裂2mol共价键 |
19.化学与日常生活密切相关,下列物质的使用不涉及化学变化的是( )
| A. | 液氨用作致冷剂 | B. | 明矾用作净水剂 | ||
| C. | 用氢氟酸刻蚀石英制艺术品 | D. | 用铁质容器盛放浓硝酸 |
16.下列物质一定属于同系物的是( )
① ②
② ③
③ ④C2H4⑤CH2═CH-CH═CH2⑥C3H6
④C2H4⑤CH2═CH-CH═CH2⑥C3H6
⑦ ⑧
⑧
①
 ②
② ③
③ ④C2H4⑤CH2═CH-CH═CH2⑥C3H6
④C2H4⑤CH2═CH-CH═CH2⑥C3H6⑦
 ⑧
⑧
| A. | ⑤⑦ | B. | ④⑥ | C. | ⑥⑧ | D. | ①③ |