��Ŀ����
3����ҵ�����õ�����ࣨ��Ҫ����Fe2O3��CuO��Cr2O3�������������ʣ�����ͭ���Ƚ���������������ͼ1��
��֪�������ʳ�����pH��CaSO4���ܽ��������ͼ2��
| Fe3+ | Cu2+ | Cr3+ | |
| ��ʼ����pH | 2.1 | 4.7 | 4.3 |
| ��ȫ����pH | 3.2 | 6.7 | a |
�ټ���ʯ�������pH��Լ3.2������Fe3+�Ѿ������IJ�����ȡ������Һ����KSCN��Һ��������죬��˵��Fe3+�ѳ�����
�ڽ���Һ���ȵ� 80�棬���ȹ���
��2��д����ԭ�����м���NaHSO3����Cu2O���巴Ӧ�����ӷ���ʽ2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+��
��3��������Ũ��С�ڻ����1��10-5 mol•L-1ʱ����Ϊ������ȫ����ҪʹCr3+��ȫ������Ҫ����c��OH-����4.0��10-9mol•L-1��[��֪��Ksp[Cr��OH��3]=6.3��10-31��$\root{3}{63}$��4.0]��
���� �������м���ϡ���ᣬ������ӦFe2O3+3H2SO4=Fe2��SO4��3+3H2O��CuO+H2SO4=CuSO4+H2O��Cr2O3+3H2SO4=Cr2��SO4��3+3H2O��Ȼ����˵õ�����I����Һ����Һ������ΪFe2��SO4��3��Cr2��SO4��3��CuSO4������Һ�м���Ca��OH��2����������ҺpH����������ͼ����Һ�к���Cr3+��Cu2+������ Fe3+��˵������II�к���Fe��OH��3�����������������Գ���II�ɷ�ΪFe��OH��3��CaSO4��ҪʹCr3+��Cu2+��������Fe3+���������������������ɳ�����ҪpHֵ֪����Һ��pH��ΧΪ3.2-4.3֮�䣻����Һ�м���NaHSO3�����������ƾ��л�ԭ�ԡ�ͭ���Ӿ��������ԣ����߷���������ԭ��Ӧ���������ש��ɫ����Cu2O�������������������ӷ�Ӧ���ɶ����������ӷ���ʽΪ2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+��HSO3-+H+=SO2��+H2O�����˵õ�Cu2O������Һ�м���NaOH��������ҺpH��������ӦCr3++3OH-=Cr��OH��3������ҺX�к���NaOH��Na2SO4���ݴ˷������
��� �⣺�������м���ϡ���ᣬ������ӦFe2O3+3H2SO4=Fe2��SO4��3+3H2O��CuO+H2SO4=CuSO4+H2O��Cr2O3+3H2SO4=Cr2��SO4��3+3H2O��Ȼ����˵õ�����I����Һ����Һ������ΪFe2��SO4��3��Cr2��SO4��3��CuSO4������Һ�м���Ca��OH��2����������ҺpH����������ͼ����Һ�к���Cr3+��Cu2+������ Fe3+��˵������II�к���Fe��OH��3�����������������Գ���II�ɷ�ΪFe��OH��3��CaSO4��ҪʹCr3+��Cu2+��������Fe3+���������������������ɳ�����ҪpHֵ֪����Һ��pH��ΧΪ3.2-4.3֮�䣻����Һ�м���NaHSO3�����������ƾ��л�ԭ�ԡ�ͭ���Ӿ��������ԣ����߷���������ԭ��Ӧ���������ש��ɫ����Cu2O�������������������ӷ�Ӧ���ɶ����������ӷ���ʽΪ2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+��HSO3-+H+=SO2��+H2O�����˵õ�Cu2O������Һ�м���NaOH��������ҺpH��������ӦCr3++3OH-=Cr��OH��3������ҺX�к���NaOH��Na2SO4��
��1���ٸ���ͼ����֪��������ȫ����pHΪ3.2��Cr3+��ʼ������pHΪ4.3�������ڳ��������У���Ҫ��ȥFe3+��CaSO4���ֲ���ʹ��Cr3+��������ز������ټ���ʯ�������pH��3.2��4.3֮�䣬����Fe3+�������軯����Һ����Һ�Ƿ��죬�ʴ�Ϊ��3.2�� ȡ������Һ����KSCN��Һ��������죬��˵��Fe3+�ѳ������ڽ���Һ���ȵ�80�棬��ͼ2��֪��80��ʱCaSO4���ܽ��Խ�С������Ҫ���ȹ��˿��Գ�ȥCaSO4���ʴ�Ϊ�����ȹ��ˣ�
��2������������Ӿ���ǿ�Ļ�ԭ�ԣ��ܺ�ͭ����֮�䷢����Ӧ��������������Լ�������ͭ�������ķ�ӦΪ��2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+���ʴ�Ϊ��2H2O+HSO3-+2Cu2+=Cu2O��+SO42-+5H+��
��3��������Ũ�ȡ�1��10-5 mol•L-1��Ϊ������ȫ����ҪʹCr3+��ȫ������Ҫ����c��OH-����$\root{3}{\frac{Ksp}{c��C{r}^{3+}��}}$=$\root{3}{\frac{6.31��1{0}^{-31}}{1��1{0}^{-5}}}$=4.0��10-9 mol•L-1���ʴ�Ϊ��4.0��10-9 mol•L-1��
���� ���⿼�����ʵķ�����ᴿ�ۺ�Ӧ�ã�Ϊ�߿���Ƶ�㣬�漰��������ܽ�ƽ�⡢����ʵ�������֪ʶ�㣬���ؿ�����������㼰ʵ�������������Ϥ����ͼ���漰�ķ�Ӧ�������������ѵ����ܶȻ��������㣮

 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д� Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�| A�� | �����ʵķ���Ƕ������������䷽�еġ�������Ρ���Ϊ�� | |
| B�� | ���ù��̷����ķ�ӦΪ������ԭ��Ӧ | |
| C�� | ���ù��̷����ķ�Ӧ�У���Ӧ����������Ϊ����� | |
| D�� | ��Ӧ�����ӷ���ʽΪ2Al3++3CO32-�T2Al��OH��3��+3CO2�� |
| A�� | ij���ʲ�������ʣ������ڷǵ���� | |
| B�� | SO3����ˮ�ɵ��磬SO3���ڵ���� | |
| C�� | �ܵ�����������ڵ���ʣ�NaCl���ڵ���ʣ�NaCl����ɵ��� | |
| D�� | ��֪������������״̬���ܵ��磬��������������״̬���ܵ��� |
 �±���������Ԫ�ص������Ϣ������������Ϣ��գ�
�±���������Ԫ�ص������Ϣ������������Ϣ��գ�| Ԫ�� | �����Ϣ |
| T | ��̬ԭ��2p�ܼ���3�������� |
| W | ��̬ԭ��p����ϳɶԵ���������δ�ɶԵ����� |
| X | �⻯�ﳣ���ڿ�ʴ���� |
| Y | ��̬ԭ�Ӻ�����ӷִ�6����ͬ�ܼ�����ÿ���ܼ��������� |
| Z | ԭ����������X��Y��ԭ������֮�� |
��2��42gT�ĵ��ʷ����Цм��ĸ���Ϊ3NA����T������⻯�������Tԭ�ӵ��ӻ�������sp3���о���Ԥ��ϳ�һ��������TԪ����ɵ�������T5+T3-����T5+������ÿ����ԭ�Ӿ�����8�����ҳʶԳƽṹ�������й�T5+�Ʋ���ȷ����BD������ţ�
A��N5+��24������
B��N5+���������������������
C��N5+�����д�������δ�ɼ��ĵ��Ӷ�
D��N3-���ӵĿռ乹��Ϊֱ����
��3��TX3��һ����ɫ����ζ�����Ҳ���ȼ�����壬�ڰ뵼��ӹ���̫���ܵ�������Һ����ʾ�������еõ��㷺Ӧ�ã�������Z���ʵĴ���������X2������TH3��Ӧ�õ�����д���÷�Ӧ�Ļ�ѧ����ʽ��4NH3+3F2$\frac{\underline{\;Cu\;}}{\;}$NF3+3NH4F���ڸ÷�Ӧ����ʽ�еļ������������ľ���������acd������ţ���
a�����Ӿ��� b��ԭ�Ӿ��� c�����Ӿ��� d����������
��4��T��W��X 3��Ԫ�صĵ縺���ɴ�С��˳��ΪF��O��N����Ԫ�ط��ű�ʾ����
��5��Z2+����T���⻯��д����λ��Ϊ4��������[Z��TH3��4]2+���������Ӿ��жԳƵĿռ乹�ͣ��������е�����TH3������Clȡ��ֻ�ܵõ�һ�ֲ����[Z��TH3��4]2+�Ŀռ乹��Ϊ�������壮
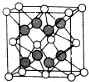
��6��X��Y�γɵĻ�����ľ����ṹ��ͼ��ʾ����֪������ܶ�Ϊ�� g•cm-3�������ӵ�����ΪNA�����߳�a=$\root{3}{\frac{312��}{{N}_{A}}}$cm�����æѡ�NA�ļ���ʽ��ʾ����
 ʵ�����ù���NaOH����0.5mol/L��NaOH��Һ500mL����������������Ʒ�У����ձ� ��100mL��Ͳ ������ƿ ��ҩ�� �ݲ����� ��������ƽ�������룩
ʵ�����ù���NaOH����0.5mol/L��NaOH��Һ500mL����������������Ʒ�У����ձ� ��100mL��Ͳ ������ƿ ��ҩ�� �ݲ����� ��������ƽ�������룩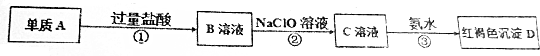
 ��
��