题目内容
12.在常温下,将4.0克氢氧化钠固体溶于水形成1L的溶液A,在A溶液中通入二氧化碳气体形成钠盐溶液.请问,A溶液的pH=13,A溶液最多能吸收该条件下的二氧化碳气体质量4.4g.(不考虑二氧化碳与水的反应及溶解)分析 根据n=$\frac{m}{M}$计算出4.0g氢氧化钠的物质的量,最高价c=$\frac{n}{V}$计算出氢氧化钠的浓度,从而可计算出该氢氧化钠溶液的pH;当生成碳酸氢钠时消耗二氧化碳的质量最大,根据质量守恒计算出消耗二氧化碳的质量.
解答 解:4.0g NaOH的物质的量为:n(NaOH)=$\frac{4.0g}{40g/mol}$=0.1mol,所得氢氧化钠溶液的物质的量浓度为:c(NaOH)=$\frac{0.1mol}{1L}$=0.1mol/L,氢氧化钠为强电解质,则溶液中氢氧根离子的浓度为0.1mol/L,该溶液中氢离子浓度为:1×10-13mol/L,该溶液的pH=13;
在A溶液中通入二氧化碳气体形成钠盐溶液,当生成碳酸氢钠时消耗二氧化碳的质量最大,根据C、Na原子守恒可知最多消耗二氧化碳的物质的量为:n(NaHCO3)=n(CO2)=n(NaOH)=0.1mol,消耗二氧化碳的最大质量为:44g/mol×0.1mol=4.4g,
故答案为:13;4.4.
点评 本题考查了物质的量的计算,题目难度不大,明确溶液pH的概念及表达式为解答关键,注意掌握物质的量与物质的量浓度、摩尔质量之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
13.下列解释事实的方程式不正确的是( )
| A. | Fe2O3溶于氢碘酸溶液中:Fe2O3+6H+═2Fe3++3H2O | |
| B. | Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| C. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | 在Cu2O固体中加入足量的稀硫酸:Cu2O+2H+═Cu+Cu2++H2O |
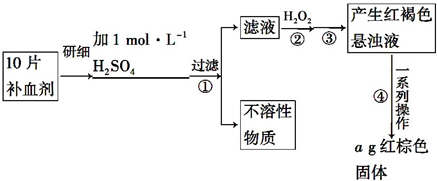
3.工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如图1:

已知部分物质沉淀的pH及CaSO4的溶解度曲线如图2:
(1)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH到约3.2,检验Fe3+已经除尽的操作是取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除尽;
②将浊液加热到 80℃,趁热过滤
(2)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+,
(3)当离子浓度小于或等于1×10-5 mol•L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥4.0×10-9mol•L-1.[已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{63}$≈4.0].

已知部分物质沉淀的pH及CaSO4的溶解度曲线如图2:
| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
①加入石灰乳调节pH到约3.2,检验Fe3+已经除尽的操作是取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除尽;
②将浊液加热到 80℃,趁热过滤
(2)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+,
(3)当离子浓度小于或等于1×10-5 mol•L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥4.0×10-9mol•L-1.[已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{63}$≈4.0].
20.曲线a和b是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述中正确的是( )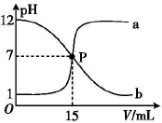

| A. | 盐酸的物质的量浓度与NaOH溶液的物质的量浓度相等 | |
| B. | P点时溶液中c(Na+)=c(Cl-)=c(H+)=c(OH-) | |
| C. | 曲线a是盐酸滴定氢氧化钠溶液的滴定曲线 | |
| D. | 曲线b中滴定前NaOH溶液的体积为150mL |
7.经研究发现有一种磷分子具有链状结构 ,下列说法不正确的是( )
,下列说法不正确的是( )
 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | 是一种极性分子易溶于水 | |
| B. | 分子中,每个磷原子以3个共价键结合3个磷原子 | |
| C. | 相对分子质量8倍于白磷分子 | |
| D. | 它和白磷都是磷的同素异形体 |
2.下列叙述中不正确的是( )
| A. | P4和NO2都是共价化合物 | B. | 在SiO2晶体中,不存在单个小分子 | ||
| C. | CCl4是以极性键结合的非极性分子 | D. | 二氯甲烷不存在同分异构体 |