题目内容
1.室温下,在pH=12的强碱溶液中,由水电离出的c(OH-)为( )| A. | 1.0×10-7mol•L-1 | B. | 1.0×10-6mol•L-1 | ||
| C. | 1.0×10-2mol•L-1 | D. | 1.0×10-12mol•L-1 |
分析 室温时,Kw=1×10-14,根据c(H+)×c(OH-)=1×10-14,以及H2O?H++OH-计算.
解答 解:室温时,Kw=1×10-14,则
pH=12的某溶液中c(OH-)=1×10-2mol/L,可碱溶液中,根据c(H+)×c(OH-)=1×10-14,
则c(H+)=1×10-12mol/L,
又H2O?H++OH-,
则由水电离的c(OH-)=c(H+)=1×10-12mol/L,
如为水解呈碱性的溶液,则由水电离的c(OH-)=1×10-12mol/L,
故选D.
点评 本题考查PH的简单计算和水的电离问题,题目难度不大,注意溶液中PH的计算方法和水的电离特点.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
13.高铁的快速发展方便了我们的出行.工业上用铝热反应 (2A1+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+A12O3)焊接钢轨间的缝隙.在反应中,Fe2O3( )
| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂也是还原剂 | D. | 既不是氧化剂也不是还原剂 |
10.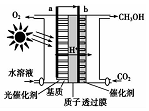 科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )
科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )
 科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )
科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )| A. | 该新型电池仅存在化学能与电能的转化 | |
| B. | 电池总反应为2CO2+4H2O=2CH3OH+3O2 | |
| C. | 电子从电极b流向电极a | |
| D. | 产生标准状况下2.24 LO2,转移电子0.6NA |
17.Na2O2、Cl2、SO2等均能使品红溶液褪色.下列说法正确的是( )
| A. | Na2O2、Cl2、SO2使品红溶液褪色原理不同 | |
| B. | Na2O2和SO2反应时,过氧化钠既作氧化剂又作还原剂 | |
| C. | 为了褪色更快,可同时向品红溶液通入等物质的量Cl2和SO2 | |
| D. | 可用H2S溶液来区别Cl2和SO2 |
6.原子团SCN化合价为-1价,在很多方面跟卤素原子相似,称为“拟卤素”.拟卤素离子与卤素离子还原性强弱顺序为Cl-<Br-<SCN-<I-.下列反应错误的是( )
| A. | (SCN)2+2NaOH→NaSCN+NaSCNO+H2O | B. | (SCN)2+2NaBr→Br2+2NaSCN | ||
| C. | 4HSCN+MnO2→Mn(SCN)2+(SCN)2+2H2O | D. | (SCN)2+2KI→2KSCN+I2 |
10.由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎,下图是氢氧燃料电池驱动LED发光的装置.下列有关叙述正确的是( )
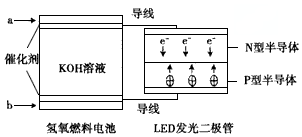

| A. | 电池负极电极反应式为H2-2e-+2OH-=2H2O | |
| B. | a处通入氧气,b处通入氢气 | |
| C. | 该装置中能量转化只涉及两种形式的能量 | |
| D. | P一型半导体连接的是电池负极 |
11.用下列有关实验装置进行相应实验,能达到实验目的是( )
| A. |  如图:配制0.10 mol•L-1NaOH的溶液 | |
| B. |  如图:除氯气中的氯化氢气体 | |
| C. |  如图:制备氢氧化铁胶体 | |
| D. |  如图:用装置④陶瓷坩埚高温煅烧CaCO3固体 |